Abstract
Multiple logistic regressions were conducted to identify the quantitative and qualitative environmental variables that best predict the occurrence of the different species of culicid mosquitoes (Diptera: Culicidae) collected over four years of study (2005-2008) in the eastern Iberian Peninsula. The results show that some variables make it possible to achieve optimal percent incidence for the species Ochlerotatus caspius, Culex pipiens, Culex territans and Culiseta longiareolata. The study of possible predictive elements for the occurrence of culicids is postulated as a useful and convenient tool for the establishment of successful mosquito population control programs.
Introducción
Profundizar en el conocimiento de los factores ambientales que afectan a la ocurrencia de las diferentes especies de mosquitos (Diptera: Culicidae) es sumamente importante para el desarrollo de exitosos programas de control poblacional (Axtell 1979; Bueno Marí y Jiménez Peydró 2011). En este sentido, existen diversos estudios que se basan en el empleo de regresiones logísticas para predecir la incidencia de los culícidos a partir de diversas variables ambientales (Udevitz et al. 1987), sobre todo aquéllas relacionadas con las características físicas y químicas de los biotopos larvarios (Vniska y Pappas 1984; Blaustein y Margalit 1995; Sunish y Reuben 2001). Con la finalidad de profundizar en el conocimiento de estas cuestiones y aportar información interesante acerca de las variables que mejoren la predictibilidad de la ocurrencia de los culícidos mediterráneos, se investigaron las poblaciones larvarias presentes en el Levante español de estos dípteros nematóceros. El objetivo fue establecer qué variables cuantitativas y cualitativas de los biotopos larvarios se asocian mejor con la presencia de las distintas especies.
Materiales y Métodos
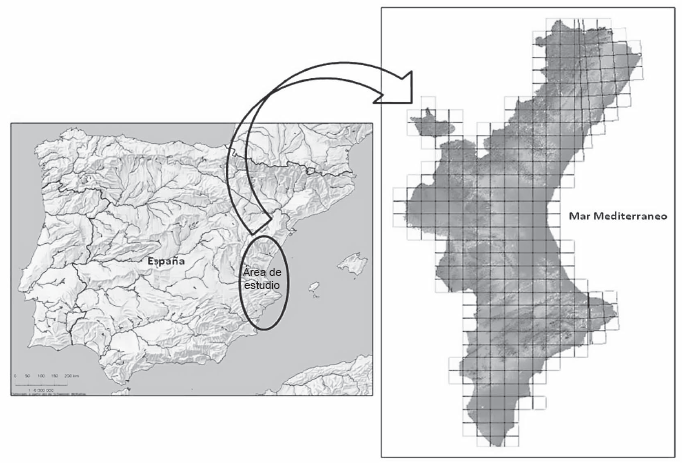
Ubicación del área de estudio.
— Tipo de ambiente acuático
° Léntico
° Lótico
— Tipo de cuerpo de agua
° Río/arroyo/riachuelo/escorrentía
° Laguna temporal o permanente
° Embalse
° Encharcamiento temporal/arrozal/zona de marismas
° Canal o acequia
° Gran receptáculo: albergan cantidades de agua superiores a 10 litros (balsa, bidón, fuente, abrevadero, pozo, piscina,…)
° Pequeño recipiente: albergan cantidades de agua inferiores a 10 litros (cubo, macetero, neumático,…)
— Tipo de sustrato (se considera el mayoritario en el biotopo en caso de coexistencia)
° Rocoso
° Pedregoso
° Arenoso
° Cenagoso
° Hormigón
° Plástico/caucho/metal
— Profundidad del foco (medición en el punto más profundo muestreado)
° Aguas someras (menos de 40 cm)
° Aguas profundas (más de 40 cm)
— Grado de antropización del ambiente
° Bajo (medios naturales o salvajes, sin actividad humana aparente en áreas circundantes)
° Medio (medios rurales, agrícolas o ganaderos que impliquen cierta actividad o asentamientos humanos en sus alrededores)
° Alto (medios urbanos o periurbanos)
Dados los beneficios reportados a partir de la dicotomización (Aguayo Canela y Lora Monge 2007) de las variables continuas (físicas y químicas del agua y altitud del biotopo) y de las categóricas policotómicas (variables cualitativas de foco acuático), se decidió transformar a sistema binario (0/1) todas las variables observadas (Tabla 1).
Variables continuas categorizadas para su dicotomización.
Nota: la media hace referencia a los valores obtenidos en la totalidad de nuestro estudio.
Puesto que la decisión acerca de la inclusión definitiva de una variable en la ecuación depende únicamente de los criterios establecidos del investigador, debido a la ausencia de pruebas estadísticas al respecto, se emplearon las pautas propuestas por Aguayo y Lora (2007) para decidir qué variables quedaban incluidas en el modelo de predicción. Por tanto fueron incorporadas aquellas variables que al ser introducidas:
— Modificaron el valor de la "estimación de la medida de asociación" (Exp(B)) de la variable principal de forma considerable (la mayoría de autores afirman que este cambio debe ser de, al menos, un 10% del valor original).
— No aumentaron sustancialmente los intervalos de confianza de la Exp(B) de la variable principal, puesto que de lo contrario habría aumentado la imprecisión de la estimación.
— No cambiaron la significación estadística del contraste de Wald para el coeficiente de regresión de la variable principal.
— Presentaron un intervalo de confianza al 95% que no contenía el valor nulo (= 1).
En el presente trabajo se muestran los datos referentes a las especies de las cuales se obtuvieron óptimos valores predictivos de su incidencia. Estos valores se fijaron en un mínimo de 50%, de manera que únicamente se aportan los modelos de predicción que han permitido pronosticar correctamente por encima del 50% de las ausencias y presencias de cada especie. Además, de los múltiples modelos probados se seleccionó para cada especie aquel con mayor poder de predicción y más parsimonioso o con menor número de variables incluidas. Las especies limnodendrófilas no fueron analizadas debido a que su carácter arborícola estricto enmascara cualquier otra variable del criadero larvario que quiera utilizarse como predictora.
Resultados y Discusión
Se identificaron un total de 679 criaderos larvarios y se capturaron 11.279 ejemplares de culícidos pertenecientes a 29 especies así: Anopheles algeriensis Theobald, 1903, Anopheles atroparvus Van Thiel, 1927, Anopheles claviger (Meigen, 1804), Anopheles maculipennis Meigen, 1818, Anopheles marteri Senevet & Prunnelle, 1927, Anopheles petragnani Del Vecchio, 1939, Anopheles plumbeus Stephens, 1828, Aedes vexans (Meigen, 1830), Aedes vittatus (Bigot, 1861), Ochlerotatus echinus (Edwards, 1920), Ochlerotatus geniculatus (Olivier, 1791), Ochlerotatus gilcolladoi (SánchezCovisa, Rodriguez & Guillén, 1985), Ochlerotatus berlandi (Séguy, 1921), Ochlerotatus caspius (Pallas, 1771), Ochlerotatus detritus (Haliday, 1833), Ochlerotatus pulcritarsis (Rondani, 1872), Culex modestus Ficalbi, 1889, Culex laticinctus Edwards, 1913, Culex mimeticus Noe, 1899, Culex pipiens Linnaeus, 1758, Culex theileri Theobald, 1903, Culex hortensis Ficalbi, 1889, Culex impudicus Ficalbi, 1890, Culex territans Walker, 1856, Culiseta longiareolata (Macquart, 1838), Culiseta annulata (Schrank, 1776), Culiseta subochrea (Edwards, 1921), Orthopodomyia pulcripalpis (Rondani, 1872) y Uranotaenia unguiculata Edwards, 1913. Sin embargo, únicamente se obtuvieron óptimos porcentajes acerca de las siguientes cuatro especies:
— Oc. caspius: especie paleártica muy abundante en terrenos pantanosos costeros (Edwards 1921; Rioux 1958) gracias a su destacada resistencia frente a la salinidad del agua, pudiendo incluso desarrollarse en ambientes hipersalinos, influenciados por la evaporación, con concentraciones de hasta 106 g/l (López Sánchez 1989). Es multivoltina, exófila, exofágica, eurígama y sus huevos resisten la desecación y las temperaturas extremas, siendo, consecuentemente habituales, los estados hibernante y estivante. La abundancia y distribución de estos huevos en medios concretos parece guardar cierta relación con el tipo de vegetación predominante, la cual se utilizaría como un elemento indicativo y fiable de las condiciones ambientales (López Sánchez 1989). Las hembras se alimentan preferentemente en horas diurnas, picando con gran agresividad y frecuencia al ser humano, y pueden desplazarse hasta 40 kilómetros en busca de hospedadores adecuados (Schaffner et al. 2001). Su interés vectorial es extenso, englobando a la transmisión de filarias (Aranda et al. 1998) y arbovirus como West Nile o Tahyna (Schaffner et al. 2001).
La inclusión de las variables "TDS alto" y "Encharcamientos" en la ecuación de regresión permitió la correcta predicción de la presencia de Oc. capius en un 67,2 % de los casos (Tablas 2 y 3). Ambas variables están íntimamente relacionadas con las características bioecológicas descritas para la especie ya que Oc. caspius tiende a anidar en ambientes de intermitencia hídrica de elevada salinidad (Bueno Marí 2011).
Valores observados y pronosticados acerca de la ausencia (0) y presencia (1) de Oc. caspius.
Variables presentes en la ecuación en cada paso incorporado y principales estadísticos asociados. Datos referentes a Oc. caspius.
Variables incorporadas en cada paso.
— Cx. pipiens: Especie distribuida por toda la región Holártica, el este y sudeste de África y Sudamérica (Stone et al. 1959). Es multivoltina, pudiendo completar hasta seis ciclos gonotróficos y, dada su ubicuidad, también es conocida como el "mosquito común". Su adaptabilidad a los ambientes urbanos, unida a su elevada endofilia, le permite ser una especie muy frecuente en el interior de las viviendas, picando ávidamente al ser humano durante la noche. Es capaz de transmitir numerosos arbovirus, tales como West Nile, Sindbis, Tahyna, Batai y Usutu, además de filarias como Dirofilaria immitis (Leidy, 1856) y plasmodios de afección aviar (Aranda et al. 1998; Schaffner et al. 2001; Bueno Marí y Jiménez Peydró 2010).
Las regresiones logísticas revelan que los "canales y acequias" "oligosalobres" caracterizados por una "antropización alta", permiten el correcto pronóstico de la presencia de Cx. pipiens en el 60% de los casos estudiados (Tablas 4 y 5).
Valores observados y pronosticados acerca de la ausencia (0) y presencia (1) de Cx. pipiens.
Variables presentes en la ecuación en cada paso incorporado y principales estadísticos asociados. Datos referentes a Cx. pipiens.
Variables incorporadas en cada paso.
— Cx. territans: Especie propia de la región Holártica ampliamente representada en el continente europeo (Horsfall 1972). Es multivoltina, eurígama y típicamente asociada a ambientes montañosos (Bueno Marí et al. 2009). Las hembras hibernan en cavidades tanto naturales como antrópicas, pican a reptiles y anfibios, y transmiten filarias de afección en batracios (Encinas Grandes 1982; Schäefer 2004).
Los ambientes fluviales "ríos o arroyos" de baja salinidad "dulces o hiposalinos" posibilitaron pronosticar con éxito la presencia de Cx. territans en el 60% de los casos (Tablas 6 y 7). Al respecto cabe señalar que Petersen y Chapman (1969) y Vniska y Pappas (1984), también evidenciaron una elevada asociación de Cx. territans con cuerpos hídricos de baja salinidad.
Valores observados y pronosticados acerca de la ausencia (0) y presencia (1) de Cx. territans.
Variables presentes en la ecuación en cada paso incorporado y principales estadísticos asociados. Datos referentes a Cx. territans.
Variables incorporadas en cada paso.
— Cs. longiareolata: Especie de distribución paleártica, oriental y afro-tropical (Schaffner et al. 2001). En Europa su presencia es más común en los países mediterráneos, siendo excepcionales sus hallazgos en regiones más norteñas del continente. Es multivoltina, estenógama, autógena, sus hábitats larvarios son muy variados y, mientras en regiones templadas hiberna en estado larvario; en áreas más frías son las hembras quienes se encargan de la supervivencia de la especie durante el periodo desfavorable (Encinas Grandes 1982; Schaffner et al. 2001). Se han descrito casos de canibalismo en larvas L4 de Cs. longiareolata, alimentándose de estados larvarios menos desarrollados de la misma u otras especies o incluso también de adultos en los momentos previos a su emergencia (Al-Saadi y Mohsen 1988). Sus preferencias hematofágicas parecen dirigirse hacia las aves, aunque ocasionalmente piquen también al hombre, y pueden transmitir el paludismo aviar y el Virus West Nile (Schaffner et al. 2001). Las variables cualitativas "Gran receptáculo" y "Sustrato plástico" permitieron predecir correctamente el 67% de las presencias de Cs. longiareolata (Tablas 8 y 9). Por tanto, se ratifica la predilección de la especie por desarrollar su etapa preimaginal en recipientes que habitualmente se encuentran en entornos domésticos o peridomésticos (Bueno Marí et al. 2010). La no inclusión de variables químicas del agua en el modelo predictivo, está en concordancia con investigaciones realizadas por otros investigadores que sugieren que la especie es euriónica y eurihalina (Dimentman y Margalit 1981; Margalit et al. 1988).
Valores observados y pronosticados acerca de la ausencia (0) y presencia (1) de Cs. longiareolata.
Variables presentes en la ecuación en cada paso incorporado y principales estadísticos asociados. Datos referentes a Cs. longiareolata.
Variables incorporadas en cada paso.
Consideraciones Finales
Existen diferentes variables cuantificables en los biotopos larvarios de los culícidos que pueden ser utilizadas para predecir la incidencia de estos dípteros nematóceros cuyo interés sanitario es de primer orden mundial. En este sentido es necesario, no sólo profundizar en estos estudios, sino también regionalizarlos, ya que es de sobra conocido que las mismas especies pueden exhibir comportamientos claramente dispares en función de la hidrografía y clima local. En conclusión, los sistemas de predicción de mosquitos culícidos nos permiten disponer de una herramienta útil desde el punto de vista del control, ya que posibilita la identificación de criaderos de especies concretas con un elevado grado de fiabilidad.
Footnotes
Agradecimientos
Los autores agradecemos a Mario Sendra, Profesor Titular del Departamento de Estadística e Investigación Operativa de la Universitat de València, por su asesoramiento en el tratamiento estadístico de los datos. Asimismo, queremos indicar nuestra gratitud a la Conselleria de Medi Ambient, Aigua, Urbanisme i Habitatge de la Generalitat Valenciana, por la concesión de los permisos pertinentes para la captura de insectos. Por último, señalar que este trabajo ha sido financiado, en parte, por el proyecto CGL 2009-11364 (BOS) otorgado por el Ministerio de Ciencia e Innovación del Gobierno de España.
