Abstract
For more than three decades, chemical insecticides have been the principal measure to control dengue fever in the department of Atlántico, Colombia. We evaluated the status of susceptibility to insecticides that are used in public health like organophosphates, organochlorates, pyrethroids and carbamates on populations of A. aegypti in the department of Atlántico. Biological assays were performed applying the standardized methodology of the Center for Disease Control and Prevention (CDC), with diagnostic doses of deltamethrin (6.25 μg/ml), lambda-cyhalothrin (6.25 μg/ml), malathion (100 μg/ml), fenitothrion (75 μg/ml), propoxur (12.5 μg/ml) and dichlorodiphenyltrichloroethane DDT (150 μg/ml) on A. aegypti mosquitoes (F2) from the municipalities of Barranquilla, Soledad (Villa Katanga and Floresta), Malambo, Puerto Colombia and Baranoa. All the evaluated populations showed susceptibility to malathion and deltamethrin, five to fenitothrion, four to propoxur and two to lambda-cyhalothrin. All of them expressed loss of susceptibility to DDT. No significant differences were found in percent mortality between populations for malathion (P = 0.15), dichlorodiphenyltrichloroethane (P = 0.54) and deltamethrin (P = 0.99), while significant differences were found for lambda-cyhalothrin (P <<0.01), propoxur (P<0.01) and fenitothrion (P <<0.01). The application of chemical insecticides for the control of dengue fever in the department of Atlántico has generated the loss of susceptibility in populations of the mosquito vector.
Introducción
El dengue constituye un problema de salud pública con tendencia al aumento en muchos países de América (Bisset et al. 1999; Tesh 2002; Montada-Dorta et al. 2007). En Colombia la incidencia del dengue ha incrementado dramáticamente desde la reinfestación de Aedes aegypti (Linnaeus, 1762) en la década de 1960 (Ocampo y Wesson 2004; Rodríguez y De la Hoz 2005). En Colombia durante los años 2006 y 2007 se registraron 82.065 casos de dengue. De éstos, 3.334 (4,06%) se presentaron en la ciudad de Barranquilla 1.899 (2,3%) y en los demás municipios del departamento del Atlántico durante el mismo período (Rojas-Álvarez 2008).
En los países de América la aplicación de insecticidas ha sido la principal medida de control para disminuir de forma rápida las densidades poblacionales del mosquito vector (Rodríguez et al. 2003; Duque-Luna et al. 2004; Ocampo y Wesson 2004; Castro et al. 2007; Montada-Dorta et al. 2007) y esta presión de selección ejercida sobre A. aegypti ha generado la aparición de poblaciones resistentes a organoclorados, organofosforados, piretroides y carbamatos en México, Cuba, Brasil, Puerto Rico, Perú, Panamá, Venezuela y Colombia (Rodríguez et al. 1997, 2004; Rawlins 1998; Prieto et al. 2002; Macorís et al. 2003; Aparecida et al. 2004; Chávez et al. 2005; Flores et al. 2005; Álvarez et al. 2006; Pereira-Lima et al. 2006; Vargas et al. 2006; Beserra et al. 2007; Salazar et al. 2007; Fonseca-González 2008; Santacoloma 2008; Maestre et al. 2009).
Desde 1950 el departamento del Atlántico ha usado insecticidas para el control de la malaria y el dengue. El primer insecticida aplicado en el departamento fue el dicloro-difenil-tricloretano (DDT) para el control de la malaria, pero fue suspendido su uso a finales de la década de 1960 debido a los hallazgos de resistencia presentados por A. aegypti en diferentes países de América y reportados por primera vez para Colombia en la ciudad de Cúcuta (Quaterman y Schoof 1958; Brown 1986; Organización Panamericana de la Salud 2009). En 1970 se aplicó en el Departamento del Atlántico el carbamato Carbaril 85% aproximadamente por tres años y desde 1974 se han usado los organofosforados malatión, fenitrotión y temefos. En la década de los ochenta se implementó el uso de los piretroides lambdacialotrina y deltametrina y se extendió el control químico a los 22 municipios del departamento, ya que esta actividad solo se realizaba en el área urbana y rural de la ciudad de Barranquilla, capital del Atlántico.
Para el departamento del Atlántico, se desconoce el estado de la susceptibilidad en adultos de A. aegypti a insecticidas de uso en salud pública, a pesar de sus altos índices de infestación (Índice de Vivienda (IV): 6% - 22%) y del historial de aplicación de insecticidas para su control (Datos no publicados - Secretaría de Salud del Atlántico). Este departamento se considera zona de riesgo para las enfermedades de transmisión vectorial (ETV) por la ubicación de importantes puertos marítimos fluviales y aéreos de Colombia; además es uno de los departamentos de mayor desarrollo industrial de la costa caribe colombiana, concentrando grandes poblaciones humanas en su capital Barranquilla y en los municipios del área metropolitana (Maestre-Serrano et al. 2008).
La detección a tiempo de la resistencia a los insecticidas en los programas de control de ETV, es uno de los lineamientos del Ministerio de la Protección Social y del Instituto Nacional de Salud, con el fin de seleccionar los insecticidas de uso en salud pública con criterio técnico y hacer uso racional de éstos. Teniendo en cuenta lo anterior, las Secretarías de Salud del Atlántico y distrital de Barranquilla, implementaron desde el año 2007 la vigilancia de la susceptibilidad a insecticidas de interés en salud pública. El presente trabajo tiene como objetivo evaluar el estado de la susceptibilidad a insecticidas de tipo organoclorado, organofosforado, piretroide y carbamato en adultos de A. aegypti de los municipios de Barranquilla, Soledad, Malambo, Puerto Colombia y Baranoa en el Departamento del Atlántico durante el año 2007.
Materiales y métodos
Área de estudio y cepas evaluadas
El departamento del Atlántico se encuentra ubicado al norte del territorio colombiano, entre los 11° 37′16″y 10°16′N y los 74°43′ y 75°16′16′E. Cuenta con 23 municipios incluida su capital Barranquilla; tiene un área de 3.328 km2, temperatura promedio anual de 28°C y humedad relativa de 75% aproximadamente (Corporación Autónoma Regional del Atlántico 2002).
Se evaluaron seis cepas de A. aegypti procedentes de los municipios de Barranquilla (barrio La Pradera), Soledad (barrio Floresta y Villa Katanga), Malambo (barrios Bella Vista, El Carmen, Villa Esperanza, Montecarlo), Puerto Colombia (barrios Pastrana y 7 de Agosto) y Baranoa (barrio Centro); los insectos procedentes de los dos barrios del municipio de Soledad Floresta y Villa Katanga, se consideraron cepas diferentes, debido a que este municipio es el octavo más grande de Colombia. Los municipios se seleccionaron porque históricamente se caracterizan por generar aproximadamente el 80% de la incidencia del dengue en el departamento. Los barrios, dentro de cada municipio, se escogieron por presentar alta incidencia del dengue y alta presión de selección por aplicación de insecticidas químicos. El barrio la Pradera del distrito de Barranquilla históricamente ha presentado el mayor número de casos de dengue; durante los años 2006-2007 se reportaron 378 casos de dengue y un IV de 14%. El municipio de Soledad ha reportado mayor incidencia de dengue en el departamento del Atlántico después de la capital Barranquilla; en los años 2006 y 2007 reportó 639 casos de dengue y para el año 2007 un IV de 11%. Durante los años 2006 y 2007 se registraron 207 casos de dengue para el municipio de Malambo, 147 casos para Baranoa y 114 para el municipio de Puerto Colombia; para el año 2007 se reportaron IV de 22%, 11% y 6% respectivamente para cada uno de estos municipios (Datos no publicados - Secretaría de Salud del Atlántico).
Con el propósito de descartar causas de disminución de mortalidad diferentes al fenómeno biológico de pérdida de susceptibilidad, tales como mala preparación de las dosis diagnóstica o fallas en la impregnación de las botellas, en cada ensayo llevado a cabo con las cepas de campo y para la totalidad de insecticidas evaluados, se utilizó la cepa de referencia susceptible A. aegypti-Rockefeller, la cual ha sido mantenida bajo condiciones controladas de temperatura y humedad en el insectario del laboratorio de entomología médica del Laboratorio de Salud Pública (LSP) del Atlántico.
Recolección de larvas y pupas parentales de A. aegypti
En cada uno de los barrios muestreados se seleccionaron manzanas al azar en las cuales se realizaron visitas domiciliarias e inspección entomológica. En cada vivienda se inspeccionaron criaderos potenciales para formas inmaduras de A. aegypti, como albercas, canecas, llantas, floreros, entre otros.
Se recolectaron larvas y pupas, las cuales se transfirieron a frascos de 500 ml utilizando agua del mismo criadero. El material entomológico se transportó al insectario del laboratorio de entomología médica del LSP del Atlántico, donde se obtuvo la generación F2 bajo condiciones controladas de temperatura y humedad relativa.
Obtención de la F2 de A. aegypti en laboratorio
Las larvas obtenidas en campo se transfirieron a bandejas plásticas de 30,5 × 20 × 10 cm con 1,3 litros de agua reposada alimentándolas diariamente con 1gr de concentrado para perro hasta que alcanzaron el estado de pupa. Posteriormente se separaron en frascos de 700 ml de capacidad llenos con 250 ml de agua declorada hasta la emergencia del adulto; éstos se liberaron en jaulas de cría tipo gerbert de 30,5 x 30,5 x 30,5 cm. Los mosquitos machos se alimentaron con solución azucarada al 10% y las hembras se alimentaron cada tercer día con sangre de ratón (Mus musculus Linnaeus, 1758) obtenidos del bioterio del LSP del Atlántico.
Para las oviposturas, se introdujo en la jaula un vaso desechable de 3,5 onzas que contenía en su interior toallas de papel absorbente y un tercio de volumen de agua reposada. Estas toallas se retiraron cada tercer día, rotulándose con el nombre, procedencia de la cepa, fecha y generación. Los huevos se mantuvieron en cámara húmeda durante las siguientes 48 horas para su secado y posteriormente se almacenaron en recipientes plásticos herméticos. Al conseguir el número suficiente de huevos se repitió nuevamente el ciclo hasta obtener mosquitos adultos de la F2. Para evitar la contaminación de las cepas, se usaron pipetas Pasteur, bandejas, frascos y jaulas diferentes para cada una de las colonias.
Ensayos biológicos
Los ensayos biológicos se realizaron siguiendo el método de las botellas impregnadas propuesto por el Centro de Control y Prevención de Enfermedades (CDC) de Atlanta, Estados Unidos (Brogdon y McAllister 1998).
Se emplearon mosquitos hembras F2 sin alimentar de tres días de nacidas de cada una de las cepas, y se introdujeron en botellas de vidrio Schott ® de 250 ml, impregnadas previamente con 1 ml de la dosis diagnóstica para cada uno de los seis insecticidas: deltametrina (6,25 μg/ml), lambdacialotrina (6,25 μg/ml), malatión (100 μg/ml), fenitrotión (75 μg/ml), propoxur (12,5 μg/ml) y DDT (150 μg/ml). Las lecturas se realizaron a los tiempos diagnósticos establecidos en estudios previos: 15 minutos para lambdacialotrina, 45 minutos para fenitrotión y 30 minutos para deltametrina, malatión, propoxur y DDT (Fonseca-González 2008; Santacoloma 2008). Las botellas control se impregnaron con 1 ml de etanol absoluto. Se realizaron tres repeticiones, cada una de cuatro réplicas más un control.
En cada una de las botellas tratamiento y control se expusieron entre 15 y 25 hembras adultas. Se determinó la mortalidad en función del tiempo de exposición, se realizaron lecturas cada cinco minutos durante una hora, contabilizando el número de insectos vivos y muertos en cada botella. Se tuvo en cuenta el criterio de mortalidad propuesto por Brogdon y McAllister (1998): mosquitos con dificultad para volar y sostenerse al momento de rotar la botella. Se realizó corrección por fórmula de Abbott (Abbott 1925), cuando se encontró mortalidad en los controles entre el 5% y el 20% y se invalidó la prueba cuando la mortalidad superó el 20%. Los ensayos biológicos, se realizaron bajo condiciones de laboratorio, a temperatura promedio de 28°C ± 2°C y humedad relativa promedio de 70% ± 10%.
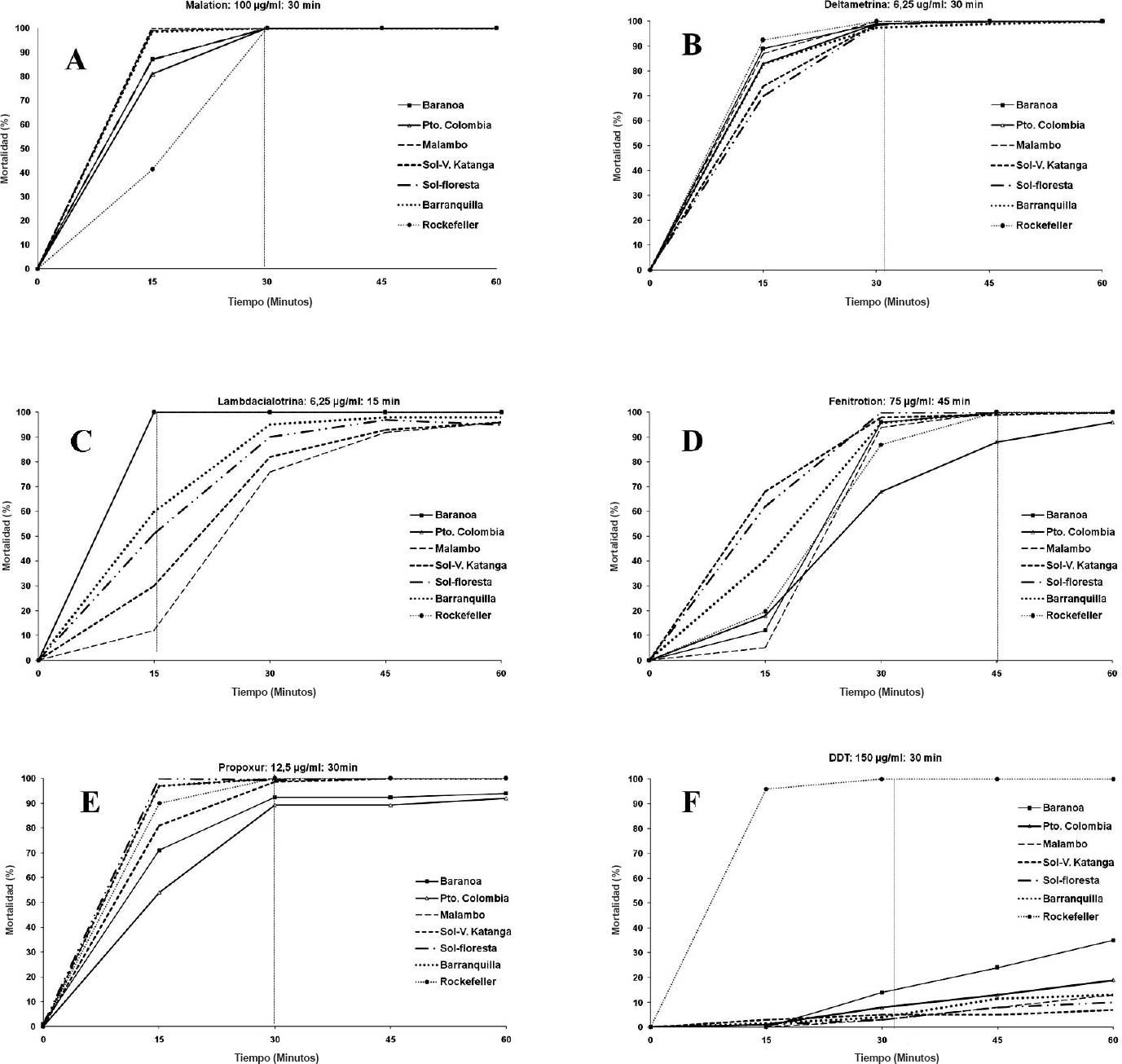
Porcentajes de mortalidad obtenidos para poblaciones de A. aegypti del departamento del Atlántico a través de la técnica CDC con dosis y tiempo diagnóstico.
Criterio de evaluación y análisis estadístico
El análisis de resultados se realizó de acuerdo con los criterios de mortalidad definidos por la metodología CDC (Brogdon y McAllister 1998), por lo tanto se consideró la población susceptible si presentaba porcentajes de mortalidad a tiempo diagnóstico entre 100 y 98% y como población con pérdida de susceptibilidad si registraba porcentajes de mortalidad a tiempo diagnóstico inferiores al 98%.
Se aplicó la prueba de Shapiro Wilk a los porcentajes de mortalidad a tiempo diagnóstico para cada insecticida en las diferentes poblaciones. Se realizó la prueba de Kruskal-Wallis al determinar que los datos no tenían distribución normal. Cuando se encontraron diferencias significativas entre poblaciones, se aplicaron pruebas no paramétricas de comparación múltiple de Tukey (Zar 1999). Se utilizó el programa Statistix 8 (Analytical Software 2003)
Resultados
Todas las poblaciones registraron susceptibilidad al malatión y a la deltametrina (Figs. 1A, B). Las cepas de Baranoa y Puerto Colombia mostraron susceptibilidad a lambdacialotrina, mientras que las cepas de Malambo, Soledad-V. Katanga, Soledad-Floresta y Barranquilla presentaron pérdida de la susceptibilidad (Fig. 1C). Todas las cepas presentaron susceptibilidad al organofosforado fenitrotión, exceptuando Puerto Colombia en la que se observó pérdida de susceptibilidad (Fig. 1D). Las cepas de Malambo, Soledad-V. Katanga, Soledad-Floresta y Barranquilla presentaron susceptibilidad al propoxur mientras que las de Baranoa y Puerto Colombia evidenciaron pérdida de susceptibilidad (Fig. 1E).
En el caso del DDT todas las cepas registraron pérdida de la susceptibilidad con mortalidades inferiores a 13,5% (Fig. 1F). No se encontraron diferencias significativas entre poblaciones para malatión (P = 0,14), DDT (P = 0,54) y deltametrina (P = 0,99); se presentaron diferencias significativas entre poblaciones para lambdacialotrina (P <<0,01), propoxur (P < 0,01) y fenitrotión (P << 0,01). Con las pruebas no paramétricas de comparación múltiple, se conformaron tres grupos de poblaciones que presentaron diferencias significativas entre sí en los porcentajes de mortalidad de las pruebas con lambdacilatronia; grupo 1: Baranoa y Puerto Colombia; grupo 2: Barranquilla, Soledad-Floresta y Soledad-V. Katanga; grupo 3: Soledad-Floresta, Soledad-V. Katanga y Malambo. Con propoxur se conformaron dos grupos que presentaron diferencias significativas entre sí; grupo 1: Barranquilla, Malambo, Soledad-Floresta, Soledad-V. Katanga y Baranoa; grupo 2: Soledad-Floresta, Soledad-V. Katanga, Baranoa y Puerto Colombia. En el caso de fenitrotión, la población de Puerto Colombia presentó diferencias significativas con respecto a las otras poblaciones evaluadas (Tabla 1).
Porcentajes de mortalidad en seis poblaciones de mosquitos de A. aegypti con su respectiva desviación estándar a dosis y a tiempo diagnóstico para cada uno de los insecticidas evaluados.
Los valores indican el promedio ± desviación estándar. Las poblaciones que tienen la misma letra no presentan diferencias significativas entre sí.
Discusión
Se registraron poblaciones de A. aegypti con pérdida de susceptibilidad a propoxur, fenitrotión, DDT y a la lambdacialotrina en el departamento del Atlántico. La pérdida de susceptibilidad en estas poblaciones probablemente se debe a la presencia de características genéticas intrínsecas de la especie que favorecen la expresión de genes de resistencia (Fonseca y Quiñones 2005; Vargas et al. 2006) y a la presión de selección ejercida por el constante uso de insecticidas químicos para el control del dengue en el departamento del Atlántico. La aparición de poblaciones de A. aegypti resistentes a insecticidas de tipo organoclorado, organofosforado y piretroide ha sido reportada por la Red Nacional de Vigilancia de la Resistencia a Insecticidas en otras regiones de Colombia tales como: Antioquia, Cundinamarca, Santander, Meta, Norte de Santander, Córdoba, Sucre, Caquetá, Guaviare, Cauca, Valle, Nariño y Chocó (Anaya et al. 2007; Salazar et al. 2007; Santacoloma 2008). Sin embargo, para el carbamato propoxur, solamente se ha encontrado pérdida de susceptibilidad en dos poblaciones correspondientes a los departamentos del Meta y Guaviare (Instituto Nacional de Salud 2010). Estos estudios han demostrado un comportamiento generalizado de la resistencia de A. aegypti al DDT en Colombia, que puede estar relacionada con la fijación de alelos resistentes y la eliminación de alelos susceptibles como consecuencia de la aplicación de este organoclorado por más de dos décadas en el país (Fonseca et al. 2009). Particularmente en el departamento del Atlántico se aplicó este insecticida hasta la década de los sesenta, lo que probablemente influyó en la resistencia al DDT encontrada en el presente estudio.
El principal motivo para incluir la evaluación de este insecticida, aunque se encuentra suspendido su uso en Colombia desde 1992, fue la posibilidad de obtener los primeros indicios de una resistencia cruzada con otros insecticidas; el DDT y los piretroides tienen el mismo mecanismo de acción, el cual consiste en el retraso en el cierre del canal del sodio y la repolarización de la membrana (Zlotkin 1999; Vontas 2001). La modificación de este sitio blanco debido a la presencia del gen kdr, conlleva a la aparición de resistencia tanto al DDT como a los piretroides. De esta manera, la presión de selección con DDT que durante tantos años presentaron las poblaciones de A. aegypti de Colombia, podría haber generado resistencia cruzada con los piretroides.
De acuerdo con lo anterior, la pérdida de la susceptibilidad a la lambdacialotrina registrada para los municipios de Barranquilla, Soledad-Villa Katanga, Soledad-Floresta y Malambo, puede estar relacionada con una resistencia cruzada al DDT, a través de mecanismos metabólicos de resistencia por incremento en las oxidasas de función mixta o al gen kdr. Estos mecanismos han sido los responsables de la resistencia en diferentes culícidos en Cuba, Perú, Guatemala y México (Brogdon y Barber 1990; Rodríguez et al. 1993, 2007; Brogdon et al. 1999; Flores et al. 2005). En Colombia se encontró asociación entre el incremento en los niveles de oxidasas de función mixta y esterasas no específicas y la resistencia registrada a DDT y a lambdacialotrina en una población de Anopheles darlingi Root, 1926, del Chocó (Fonseca et al. 2009), pero hasta el momento no se ha reportado resistencia por gen kdr en ninguna de las poblaciones de culícidos estudiadas en el país.
Los insecticidas organofosforados han sido utilizados para el control de A. aegypti durante los últimos 15 a 20 años en varios países de América. Particularmente el departamento del Atlántico inició su uso a partir de la década de los 70; sin embargo, los piretroides que han sido usados más recientemente, a partir de la década de los 80, muestran mayores niveles de resistencia en comparación con los organofosforados, a pesar del mayor tiempo de uso de estos últimos (Bisset et al. 2003). En nuestros resultados, todas las poblaciones fueron susceptibles al organofosforado malatión y al piretroide deltametrina; En relación con el organofosforado fenitrotión, únicamente la población de Puerto Colombia presentó pérdida de susceptibilidad en comparación al piretroide lambdacialotrina, que presentó esta característica en cuatro poblaciones. La pérdida de la susceptibilidad para el fenitrotión en la población de Puerto Colombia puede estar relacionada con el uso de este organofosforado en el departamento del Atlántico desde la década de los 70 o a la resistencia reportada al organofosforado temefos en A. aegypti en este municipio (Maestre et al. 2009).
Se recomienda investigar la pérdida de la susceptibilidad en las poblaciones de Baranoa y Puerto Colombia frente al carbamato propoxur, el cual es un insecticida que no ha sido aplicado desde las Secretarías de Salud del Atlántico y distrital de Barranquilla. Sin embargo, el propoxur era el ingrediente activo de un producto comercial de uso doméstico, el cual fue utilizado por mucho tiempo por las comunidades en Colombia. Se debe estudiar si esta pérdida de la susceptibilidad es resultado de una resistencia cruzada o si se debe al incremento en las oxidasas de función mixta, responsables de la resistencia a carbamatos, piretroides y DDT.
Los resultados de esta investigación, acompañados del desarrollo de pruebas de eficacia/efectividad en campo, permitirán a los programas de enfermedades de transmisión vectorial (ETV) de las Secretarías de Salud departamental, distrital de Barranquilla y municipal de Soledad, implementar estrategias de control de la patología con un criterio técnico, al escoger el insecticida a utilizar según el estado de susceptibilidad en cada una de las poblaciones evaluadas (Prieto et al. 2002). Es importante disminuir la presión de selección en las poblaciones en las que se detectó resistencia; la suspensión de los insecticidas podría conllevar a la reversión de la susceptibilidad en las poblaciones de A. aegypti; este fenómeno fue reportado en la ciudad de Cali (Colombia) en larvas de esta especie con el larvicida temefos (Prieto et al. 2002; Fonseca y Quiñones 2005).
Se considera importante ampliar este estudio determinando los mecanismos de resistencia expresados en estas poblaciones, mediante el uso de sinergistas, pruebas bioquímicas y moleculares, que permitan entender el mecanismo fisiológico que origina la resistencia en las poblaciones de A. aegypti a los insecticidas evaluados, con el fin de conocer, controlar el desarrollo y mitigar la abundancia de estas poblaciones en el departamento del Atlántico (Vargas et al. 2006). El presente trabajo contribuye al fortalecimiento de la red nacional de la vigilancia de la resistencia a insecticidas de interés en salud pública para la especie A. aegypti.
Footnotes
Agradecimientos
Queremos expresar nuestros agradecimientos a los técnicos de los programas de ETV de las Secretarías de Salud del municipio de Soledad, distrito de Barranquilla y departamento del Atlántico por la recolección del material entomológico en cada uno de los municipios evaluados. A la técnico de laboratorio Lisceth Hanner Maestre por su colaboración en el manejo y mantenimiento de las cepas de A. aegypti. A la Gobernación del Atlántico – Secretaría de Salud y el Instituto Nacional de Salud – Laboratorio de Entomología por la financiación del presente trabajo de investigación.
