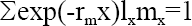Abstract
The geminiviruses of cassava mosaic virus (CMGs) (Geminiviridae, Begomovirus) and their whitefly vector, Bemisia tabaci, produce the major losses in root yield of cassava crops in Asia and Africa. Recent evidence suggests that B. tabaci represents a complex of morphologically indistinguishable populations with numerous biotypes. In the Americas, although cassava seems not to be a suitable host for the polyphagous biotype B, it has being postulated that the absence of CMGs and the mechanical damage are related with incapability of this biotype to colonize efficiently this crop. However, previous studies have demonstrated that their adaptation to cassava, via alternate hosts, is a risk that must always be kept in mind. The main objective of this study was to evaluate the development and reproduction of B. tabaci biotype B feeding on three genotypes of M. esculenta (MEcu72, CG489-34 and CMC-40). Bioassays, carried out under controlled conditions (25±2°C, 70±5RH; 12:12 LD), were used to evaluate longevity, fecundity, reproduction and demographic parameters through life tables. Although mean values for longevity were similar in MEcu72, CG489-34 and CMC-40 (6.3, 5.07, and 3.9 days, respectively) CMC-40 showed the lowest oviposition rate (0.49 eggs/female/ 2days) compared with MEcu72 (0.89) and CG489-34 (0.86). With a very low survival rate (0.03), MEcu72 was the only genotype where the biotype B was able to complete its development from egg to adult, requiring 55.1 days. Results are discussed in terms of evaluating the potential adaptation of B. tabaci on commercial cassava genotypes.
Keywords
Introducción
La yuca (Manihot esculenta Crantz, 1766) contribuye significativamente a la nutrición y calidad de vida de más de 500 millones de personas, miles de procesadores y comerciantes alrededor del mundo (Balagopalan 2002). La yuca es originaria del Neotrópico aunque su centro de origen es aun motivo de discusión (Allem 2002), este hecho es consistente con la gran diversidad de artrópodos plaga que atacan este cultivo (Bellotti et al. 1994). Las moscas blancas, como plagas de alimentación directa y vectores de virus, constituyen el mayor problema para la producción de yuca en África, Neotrópicos y en menor grado Asia (Bellotti 2002). En el neotrópico, el complejo más grande de especies lo incluyen Bemisia tabaci (Gennadius, 1889), B. tuberculata (Bondar, 1923) y Trialeurodes variabilis (Quaintance, 1900). B. tabaci tiene una distribución pantropical, y en África se alimenta de yuca y transmite la enfermedad del virus del mosaico de la yuca (CMD), un complejo de ocho especies de geminivirus (CMGs) (Geminiviridae, Begomovirus) (Legg et al. 1994; CIAT 2004).
Hasta el momento, en África, el daño de B. tabaci se documenta, principalmente, por su importancia como vector de CMD pero sus poblaciones, que se han incrementado en la parte oriental y central (Uganda, Tanzania, Ruanda y República del Congo) causan, además, daño físico directo a los culti-vos de yuca. Las pérdidas en rendimiento han sido estimadas en más del 50%, incluyendo variedades con reconocida resistencia exclusiva a CMD (CIAT 2004). Estos resultados indican que cultivares de yuca con esta característica podrían no ser los más adecuados para evitar las pérdidas por daño debido a la alimentación directa de altas poblaciones de B. tabaci.
En el Neotrópico, las medidas de control en cultivos de yuca, expuestos durante un largo periodo (8-24 meses) a la presión de poblaciones de mosca blanca, se han basado en el uso de costosos insecticidas, haciendo poco rentable su producción. Adicionalmente, el hecho que yuca sea tradicionalmente sembrado en suelos marginales y pobres en nutrientes expone el cultivo a estrés e incrementa la susceptibilidad al ataque de B. tabaci (Palumbo et al. 2001; Calatayud et al. 2002).
Recientes evidencias sugieren que B. tabaci representa un complejo de poblaciones morfológicamente indistinguibles, con numerosos biotipos (Perring 2001). A pesar de la naturaleza polífaga del complejo de poblaciones de B. tabaci (Mound 1983) se conoce, además, de la existencia de poblaciones mono y oligofagas, como es el caso de los biotipos Jatropha (Brown et al. 1995), yuca (Abdullahi et al. 2003) y el biotipo B de las Américas. Esto ha sido nuevamente resaltado en estudios de transferencia de hospederos, los cuales corroboraron que el desarrollo y reproducción de poblaciones del biotipo-yuca está restringido a M. esculenta, M. glaziovii Muell.-Arg, berenjena (Solanum melongena L.) y S. aethiopicum L. (Legg et al. 1994). Así mismo, experimentos de laboratorio han mostrado que es capaz de reproducirse sobre Nicotiana debneyi Domin (Thompson 2003), Lycopersicon esculentum Mill. y Vigna unguiculata (L.) Walp (Omondi et al. 2005). En contraste, las poblaciones del biotipo no-yuca pueden colonizar un amplio rango de malezas y cultivos, a excepción de yuca. Dado que, en las Américas, yuca parece ser un hospedero inadecuado para el polífago biotipo B (reconocido por algunos investigadores como B. argentifolii Bellows y Perring) (Bellows et al. 1994), se ha postulado que la ausencia de CMGs y daño mecánico están relacionados con la inhabilidad de este biotipo para colonizar eficientemente este cultivo. No obstante, B. tabaci fue encontrada alimentándose de yuca en República Dominicana y Cuba (Brown et al. 1995; Vásquez et al. 1995), Ecuador y Colombia (Anderson et al. 2005). Además que, estudios recientes, sugieren la posibilidad de que desarrolle poblaciones sobre este cultivo, cuando se utiliza un modelo de adaptación gradual sobre una serie de hospederos filogenéticamente relacionados con Manihot (Carabalí et al. 2005). Estos antecedentes dan base a la hipótesis que poblaciones polífagas de B. tabaci (biotipo B) podrían desarrollarse y reproducirse sobre genotipos de yuca.
Ante el riesgo potencial que constituye la colonización de altas poblaciones de B. tabaci y CMD para la producción de yuca en las Américas, más aún, si se tiene en cuenta que los cultivares más tradicionales son altamente susceptibles a la enfermedad, se planteó el presente trabajo, el cual tuvo como propósito evaluar el desarrollo, reproducción y los parámetros demográficos del biotipo B de B. tabaci sobre tres genotipos de yuca (MEcu72, CG489-34 y CMC-40).
Materiales y Métodos
Biología de B. tabaci sobre genotipos de M. esculenta
Moscas blancas y plantas.
Los individuos del biotipo B fueron obtenidos de una colonia previamente establecida sobre J. gossypiifolia L. (25 ± 2°C, 70 ± 5% H. R., 12 horas de fotoperiodo) a partir de la cual, se obtuvo una cría de B. tabaci en M. carthaginensis Mueller von Arg. (Carabalí et al. 2005) que fue mantenida durante cinco generaciones en jaulas de tul y madera (1 x 1 x 1 m) bajo iguales condiciones controladas. La cepa del biotipo B de B. tabaci fue confirmada periódicamente en adultos con el análisis RAPD-PCR (Quintero et al. 2001). 20 plantas de CMC-40, MEcu72 y GC 489-34, fueron suministradas por la Unidad de Recursos genéticos del CIAT y en los experimentos se utilizaron plantas de 30 - 40 días de siembra, las cuales se multiplicaron a partir de estacas, utilizando materas plásticas de 15 cm de profundidad con capacidad aproximada para un 1 kg de suelo. Las plantas se ubicaron en una casa malla, sobre mesas de 1m de altura.
Longevidad y fecundidad de hembras.
Cuarenta parejas de machos y hembras de B. tabaci, recién emergidas y previamente sexadas, provenientes de la cría sobre M. carthaginensis se separaron en jaulas pinza (diámetro = 2,5 cm; profundidad = 2 cm). Los insectos se colocaron sobre el envés de las hojas de los genotipos MEcu72, CG489-34 y CMC-40. Cada 48 h los adultos se removieron a una nueva área de la hoja hasta la muerte natural de las hembras. Los machos se reemplazaron por otros en la medida que morían antes que su pareja. El área de la hoja bajo cada jaula pinza se marcó y observó bajo estereomicroscopio binocular (40X) para el conteo del número de huevos. La fecundidad se estimó como el número de huevos colocados por hembra cada 48 horas y la longevidad, como el máximo número de días que una hembra vive.
Tiempo de desarrollo, tasa de supervivencia y proporción de hembras.
Cincuenta adultos no sexados de B. tabaci, de dos días, se tomaron de hojas apicales de plantas de M. carthaginensis, con la ayuda de un aspirador bucal y posteriormente fueron colocados en jaulas pinza (diámetro = 2,5 cm; profundidad = 2 cm) sobre el envés de las hojas de los genotipos MEcu72, CG489-34 y CMC-40. Los adultos y las jaulas pinza se retiraron transcurridas seis horas. Con la ayuda de un estereoscopio binocular (40X), se seleccionaron al azar 200 huevos. El área demarcada con los 200 huevos fue observada diariamente para registrar el tiempo de desarrollo de huevo-adulto. La tasa de supervivencia de los estados inmaduros fue estimada, como el número de huevos iniciales que llegan adultos y la proporción de hembras emergidas.
Parámetros demográficos.
Los datos del tiempo de desarrollo, tasa de supervivencia y proporción de hembras fueron combinados con los datos experimentales de la reproducción '1-m' para producir tablas de vida. Para cada experimento se calcularon los siguientes parámetros demográficos (Price 1975): 1) Tasa de reproducción neta (R0) definida como el número de hijas que en promedio una hembra deja durante una generación; 2) Tiempo generacional (T), equivalente al periodo comprendido entre el nacimiento de los padres y el de la progenie y 3) Tasa intrínseca de crecimiento de la población (rm), la cual representa la contribución diaria de cada individuo al desarrollo poblacional. La tasa intrínseca de crecimiento de la población (rm) fue estimada mediante la ecuación:
donde: x, es la edad de la hembra
lx, edad de supervivencia específica
mx, la proporción de hembras de la progenie de una hembra con edad x.
En el cálculo del valor de (rm), se utilizó la edad corregida X + 0,5 y la ecuación In 2/rm para estimar los días necesarios para duplicar en número la población (Carey 1993).
Análisis estadístico
Los valores de la longevidad, fecundidad, tasa de oviposición y tiempo de desarrollo del biotipo B de B. tabaci en cada genotipo de M. esculenta se analizaron mediante la prueba de Kruskal-Wallis la cual permite comparar las medias de dos o más distribuciones sin el supuesto de que los términos del error se distribuyen normalmente. Cuando fue requerido, se realizaron pruebas de comparación múltiple, utilizando el método de Student-Newman-Keuls.
Resultados y Discusión
Biología de B. tabaci sobre genotipos de M. esculenta
Longevidad y fecundidad de hembras.
La longevidad de las hembras en los tres genotipos no fue significativamente diferente (Tabla 1). Sin embargo, las hembras vivieron entre uno y dos días más sobre MEc 72 en comparación con CG489-3 y CMC-40, respectivamente. Así mismo, el rango de longevidad más amplio (dos a 20 días) se presentó en MEcu 72 (Tabla 1). En contraste, las hembras vivieron menos tiempo (3,9 días) en CMC-40. Estas diferencias se pueden observar en las curvas de supervivencia (Fig. 1) donde, al sexto día la proporción de hembras vivas se redujo 60, 70 y 85% en MEcu72, CG 489-34 y CMC-40, respectivamente.
Longevidad (días), fecundidad media (huevos) y tasa de oviposición (huevos/hembra/2días) del biotipo B de B. tabaci en tres genotipos de M. esculenta (n = 40).
Promedios seguidos por diferentes letras entre las columnas difieren significativamente, (Kruskal-Wallis P < 0,0001, seguido por Student-Newman-Keuls P < 0,05). Números entre paréntesis representan los rangos.
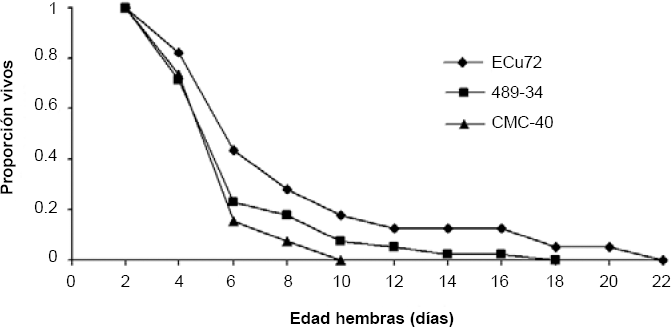
Supervivencia del biotipo B de B. tabaci en tres genotipos de Manihot esculenta.
La fecundidad media del biotipo B sobre los genotipos MEcu72 y CG489-34 fue similar entre si, pero significativamente diferentes al ser comparados con CMC-40 (Kruskal-Wallis, P < 0,0001) (Student-Newman-Keuls, P < 0,05) (Tabla 2). La más alta fecundidad (5,6 huevos) se observó en MEc72, y fue el triple al compararse con CMC-40 (Tabla 1). Además, fue en MEc 72 donde las hembras presentaron el rango más amplio de oviposición (uno a 40 huevos).
Tiempo de desarrollo, supervivencia y proporción de hembras de individuos del biotipo B de B. tabaci en MEcu72 (n = 200).
Se presentó sincronía al inicio de la oviposición (48 h) sobre los tres genotipos, sin embargo al sexto día, sobre CMC-40 las hembras ya habían ovipositado el 100% de los huevos, mientras, en MEcu72 y CG 489-34, alcanzaron el 75,8 y 75,3%, respectivamente (Fig. 2). La distribución de la secuencia de la aparente conveniencia de los genotipos en la variable fecundidad fue MEcu72 > CG489-34 > CMC-40, concordante con los del análisis de longevidad.
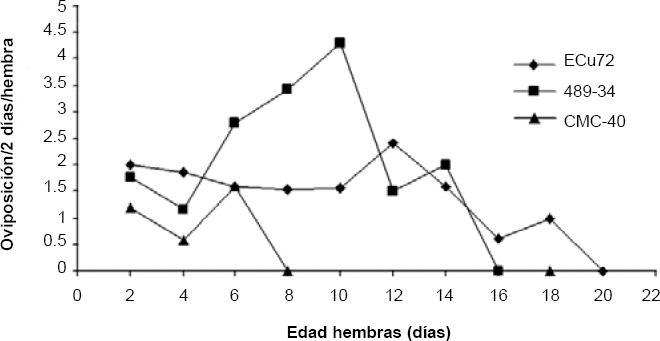
Curvas de reproducción del biotipo B de B. tabaci en tres genotipos de Manihot esculenta.
Los promedios de las tasas de oviposición de MEcu72 y CG489-34 fueron similares entre si (Tabla 1), siendo ligeramente superiores en el primer genotipo, pero significativamente diferentes al ser comparados con CMC-40 (Kruskal-Wallis P < 0,0001) (Student-Newman-Keuls, P < 0,05). Las diferencias en las tasas de oviposición media para cada genotipo se pueden observar en la figura 2, las cuales permiten predecir, en forma limitada, qué tan adecuado puede resultar cada uno de los hospederos para el posterior desarrollo de los estados ninfales. Al comparar las tasas de oviposición entre MEcu72 y CG489-34 fue evidente que no presentaron diferencias significativas, pero si al compararse con CMC-40.
Las diferencias en la oviposición de B. tabaci en cada genotipo obtenidos en este estudio concuerdan con los resultados reportados por Heather et al. (1991), quienes encontraron que cuando se confina B. tabaci a un hospedero en particular (Gossypium hirsutum L., Cucumis maxima Dúchense, C. pepo L., C. melo L., Lactuca sativa L., Lycopersicon esculentum Mill.), no deposita igual número de huevos sobre todos los hospederos. Adicionalmente, confirman que no existe una correlación directa entre el número de huevos depositados y las tasas de supervivencia. Estos resultados sugieren que las hembras de B. tabaci antes de la oviposición sobre los genotipos de M. esculenta (MEcu72, CG489-34 y CMC-40) pueden no ser capaces de identificar la potencial conveniencia del hospedero.
Tiempo de desarrollo, tasa de supervivencia y proporción de hembras.
Aunque con una tasa de supervivencia de los estados inmaduros baja (3%), MEcu72 fue el único hospedero donde el biotipo B pudo completar su desarrollo, necesitando 55,1 días para llevarlo a cabo (Tabla 2). Tanto en el genotipo CG489-34 como en CMC-40, los mayores porcentajes de mortalidad ocurrieron en el primer instar. Los sobrevivientes se desarrollaron hasta segundo y tercer instar en CG489-34 y solo hasta el segundo en CMC-40. En cada caso, las ninfas entraron en un estado de latencia sin alcanzar el estado adulto.
Los resultados de este estudio difieren a lo reportado por Costa y Russell (1975), quienes en ensayos con diferentes variedades de yuca, registraron una mortalidad del 100% de los insectos en los tres primeros días, dando soporte a que B. tabaci no se alimenta ni se reproduce sobre M. esculenta en las Américas. A diferencia de estos autores, en nuestros experimentos B. tabaci se reprodujo sobre MEcu 72 y en CG489-34 y CMC-40 este porcentaje de mortalidad se presentó en un rango de ocho a 20 días. La proporción de hembras fue afectada cuando B. tabaci se alimentó sobre MEcu72, resultado de la baja tasa de supervivencia alcanzada por la mosca blanca sobre este genotipo (Tabla 2).
Parámetros demográficos.
Como resultado de una tasa de supervivencia negativa de los estados inmaduros de B. tabaci sobre CG489-34 y CMC-40, no se pudo calcular los parámetros demográficos sobre estos hospederos. No obstante, el efecto del hospedero sobre la tasa reproductiva neta de la mosca blanca permitió estimar que, en promedio, al cabo de una generación (58,3 días), las poblaciones del biotipo B sobre MEcu72 podrían multiplicarse 5,61 veces (individuo/individuo). Así mismo, la tasa intrínseca de la población sobre MEcu72 fue baja (0,0296), siendo su potencial de crecimiento inferior en un 84%, al compararla con la tasa de crecimiento registrada por Musa y Ren (2005), sobre un hospedero conveniente como soya (Glycine max (L.)). Estos valores se reflejan en el tiempo requerido por B. tabaci para duplicar en número su población sobre MEc72, el cual fue de 23,4 días.
Es importante anotar que, en África, las poblaciones de B. tabaci asociadas a yuca han sido reportadas como monófagas (Storey y Nichols 1938; Abdullahi et al. 2003) aunque han sido detectadas también sobre plantas de Fabaceae (Centrosema molle Mart. ex Benth.) (Legg 1996), Solanaceae (Solanum nigrum L.; S. aethiopicum L.; S. melongena L.) (Burban et al. 1992), Verbenaceae (Lantana camara L.) (Legg 1996) y E. heterophylla (Miq.) Miers (Thompson 2003). Más recientemente se ha demostrado que las poblaciones de B. tabaci, tipo Ug1 (Uganda 1) consideradas especificas para yuca (Sseruwagi et al. 2006) no lo son, dada su capacidad de colonizar otras plantas, entre ellas: Aspilia africana pers. Adams, Abelmoschus esculentus L., Manihot glaziovii Muell. Arg., J. gossyipiifolia L. y Euphorbia heterophylla L. Así mismo, estudios anteriores en Uganda mostraron que ciertas poblaciones de B. tabaci que colonizan yuca, fueron capaces de sobrevivir sobre algodón (G. hirsutum L.) y batata (Ipomea batatas L.) aunque dichas poblaciones al ser transferidas a yuca no sobrevivieron (Legg 1996).
Estos hechos sugieren, que las poblaciones de B. tabaci asociadas a yuca en África podrían estar ampliando su rango de hospederos y, en consecuencia, generando una reestructuración de su monofagia. En forma similar, en las Américas, el biotipo B, conocido por su asociación a más de 600 especies de plantas hospederas (Mound y Halsey 1978; Secker et al. 1998) podría estar ampliando su rango de hospederos y entre ellos, yuca. Aunque difícil de establecer el inicio de este proceso, es posible que se opere desde 1990 cuando se observó B. tabaci colonizando yuca en República Dominicana (Brown et al. 1995) y luego, en 1993, se registró como predominante en la misma especie en Cuba (Vázquez et al. 1995) y, más reciente, en Colombia y Ecuador (Quintero et al. 1998; Anderson et al. 2005). A pesar que las poblaciones de B. tabaci presentaron un bajo potencial de desarrollo sobre el genotipo de M. esculenta MEcu72, se constituye en uno de los primeros registros experimentales en el cual el biotipo B se desarrolló sobre un genotipo comercial de M. esculenta. En consecuencia y aunque preliminares, nuestros resultados permiten sugerir que M. esculenta puede ser un hospedero potencial para el biotipo B de B. tabaci en las Américas.
Footnotes
Agradecimientos
A los evaluadores anónimos quienes a través de su revisión crítica, hicieron aportes significativos y valiosos al manuscrito.