Abstract
Among the most serious obstacles in vector control programs for human diseases is the development of resistance to the insecticides used. According to WHO, approximately 40% of the 506 medically important arthropods show some degree of insecticide resistance. Of these species, about 50% are species of mosquitoes that vector malaria, dengue, yellow fever and filariasis. The two principal mechanisms of insecticide resistance are alterations in the target site or an increase in the detoxification rate of the insecticide. Once resistance is detected in a vector population it is crucial to determine its molecular and biochemical basis. Identification of resistance mechanisms permits the selection of insecticides to use in control programs and the evaluation of potential development of resistance to alternative insecticides. This review presents basic information regarding the main mechanisms of insecticide resistance identified in mosquito vectors of human diseases and the methodologies most used to monitor and detect them.
Introducción
Cada año, millones de personas alrededor del mundo se enferman y mueren por enfermedades transmitidas por insectos vectores, como malaria, dengue, leishmaniosis y tripanosomiasis. Estas enfermedades causan gran impacto económico y social, particularmente en países tropicales como Colombia. Actualmente, ningún método efectivo de inmunización está disponible para controlar dichas enfermedades y la única forma de controlar la transmisión está dirigida hacia sus vectores. El uso de insecticidas químicos ha sido la forma más utilizada en los programas de control. Éstos se han empleado por más de 60 años con resultados variables. Inicialmente se usaron piretrinas, de corto efecto de noqueo. Posteriormente se introdujeron insecticidas de mayor acción residual como los órganoclorados, carbamatos y órganofosforados.
A partir de 1990, el desarrollo de piretroides sintéticos fotoestables y las presiones de grupos ambientalistas desplazaron el uso del DDT (Dicloro-difenil-tricloroetano) para la fumigación intradomiciliar en los programas de control de malaria, siendo en la actualidad el tipo de insecticida más usado tanto en rociamientos intradomiciliares como en la impregnación de toldillos (Lengeler et al. 1996; Phillips 2001).
En 1947, tan solo un año después de la introducción de insecticidas para el control de vectores, se notificaron los primeros casos de resistencia a DDT en Aedes tritaeniorhynchus (Weidemann) y Ae. solicitans (Walker) (Brown 1986). Desde entonces se han señalado más de 100 especies de mosquitos resistentes a uno o más insecticidas, de las cuales 56 son Anophelinos y 39 Culicinos, además de triatomineos, pulgas, piojos y garrapatas (WHO 1992). Actualmente, el Comité de Acción para la Resistencia a Insecticidas (IRAC) cita en su página web (http://www.plantprotection.org/irac) resistencia en 21 especies de Aedes, entre ellas el vector de dengue Ae. aegypti (Linnaeus) (resistente a 16 insecticidas) y 63 especies de Anopheles, incluyendo Anopheles albimanus Weidemann, An.darlingi Root, An. pseudopunctipenis Theobald y An. rangeli Gabaldon, Cova García & López, todas éstas importantes en la transmisión de malaria en Colombia.
En Colombia, la descentralización de los programas de control de malaria y dengue desde 1992 ha dificultado la vigilancia permanente del estado de la resistencia a insecticidas en las poblaciones vectoras. No obstante, existen registros de resistencia al DDT y Temefos en diferentes especies de Anopheles y Ae. aegypti en el país, respectivamente (Quiñones et al. 1987; Suárez et al. 1990), los cuales sugieren que las poblaciones de vectores presentan características genéticas favorables para la emergencia de resistencia cuando éstas sean presionadas por insecticidas. Sin embargo, debido a que no hay conocimiento de los mecanismos bioquímicos que generaron la resistencia al DDT y a otros químicos, se desconoce el impacto que podría tener el uso de otros insecticidas que compartan el mismo mecanismo de acción, causado por efectos de resistencia cruzada.
La resistencia a insecticidas o resistencia fisiológica se define como la capacidad de una población de insectos de tolerar dosis de un insecticida que serían letales para la mayoría de los individuos en una población normal de la misma especie y es el resultado de la presión de selección positiva ejercida por el insecticida (WHO 1975) sobre genes inicialmente en baja frecuencia. Los genes de resistencia pueden luego dispersarse en la población local de insectos e incluso en el mundo. Los patrones de distribución de estas variantes genéticas en poblaciones naturales son el efecto conjunto de varias fuerzas evolutivas y factores demográficos como la selección, mutación y el ciclo de vida (Gazave et al. 2001).
Numerosos factores influyen en la evolución de la resistencia a insecticidas, los cuales pueden agruparse en tres categorías: factores genéticos, biológicos y operacionales. Los factores genéticos se relacionan principalmente con la frecuencia y dominancia de los alelos de resistencia, en tanto que los biológicos incluyen el ciclo de vida, el número de descendientes por generación y las tasas de flujo génico. Los factores genéticos y biológicos son intrínsecos a las especies y por lo tanto se escapan del control humano. Los factores operacionales si pueden ser manejados a fin de evitar o retardar el desarrollo de resistencia. Estos factores se asocian directamente con el tiempo, dosis y formulación del insecticida, el estadío seleccionado y el uso previo de insecticidas relacionados (Georghiou 1990).
Mecanismos de Resistencia
Los dos principales mecanismos de resistencia a insecticidas son las alteraciones en el sitio blanco y un incremento en la tasa de detoxificación de los insecticidas. Se proponen también mecanismos basados en la respuesta al estrés térmico (Patil et al. 1996), penetración disminuida, incremento en las tasas de excreción y cambios de comportamiento que eviten el contacto con los insecticidas aunque los vectores sean susceptibles a éstos (Brogdon y McAllister 1998a).
La resistencia mediada por el sitio blanco ocurre cuando el insecticida no logra unirse a su sitio de acción ya sea porque hay disminución en la sensibilidad del sitio blanco o modificación de éste (Hemingway y Ranson 2000). La resistencia basada en enzimas detoxificantes se presenta cuando niveles elevados o actividades modificadas de estas enzimas contribuyen a disminuir la dosis efectiva de un insecticida evitando que llegue a su sitio de acción (Ranson et al. 2002a). (Fig. 1).
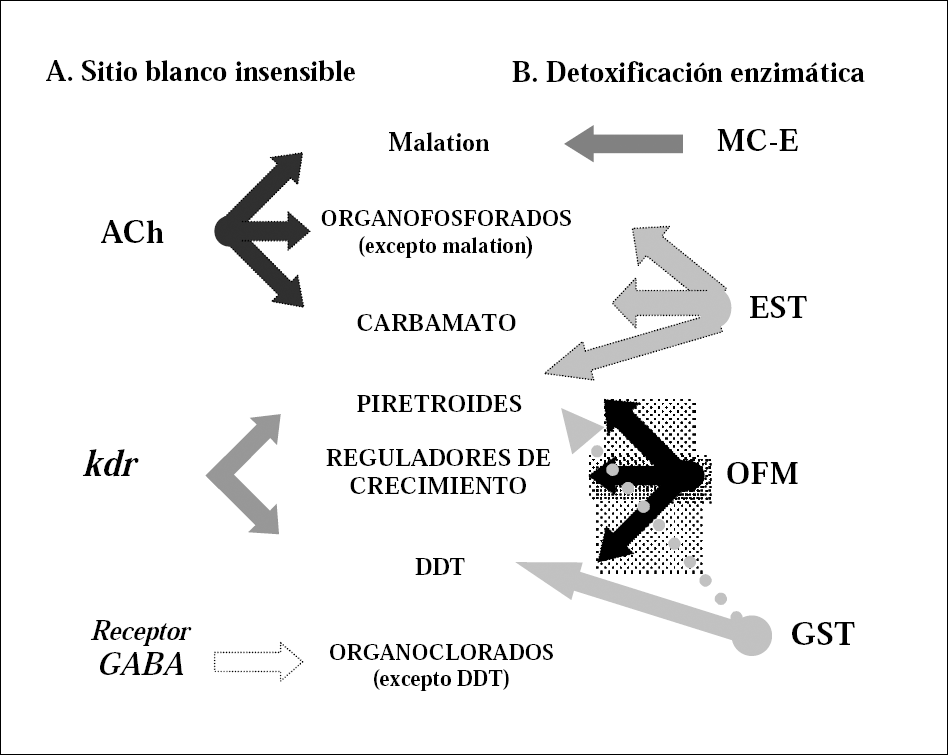
Mecanismos de Resistencia a Insecticidas. AchE: Acetilcolinestarasa Inhibida. Kdr: resistencia “Knockdown”. GST: Glutation S-transferasas. EST: Esterasas inespecíficas. OFM: Oxidasas de función mixta. MC-E: Malation carboxil-esterasas.
1. Alteraciones en el sitio blanco
La causa más común de resistencia en el sitio blanco es la presencia de mutaciones puntuales no silentes en genes estructurales. Para que dichas mutaciones sean seleccionadas favorablemente, el cambio en el aminoácido debe disminuir la unión al insecticida sin causar pérdida de la función primaria del sitio blanco. Por lo tanto, el número de posibles sustituciones de aminoácidos es limitado y comúnmente se encuentran mutaciones idénticas asociadas con resistencia a través de taxa altamente divergentes. El grado de deterioro de la función, ocasionado por la mutación que confiere resistencia, se refleja en la eficacia biológica de los individuos resistentes en ausencia de selección por el insecticida. Este costo en la eficacia biológica tiene importantes implicaciones para la persistencia de resistencia y/o reversión a la susceptibilidad en poblaciones de campo (Berticat et al. 2002).
1.1. Cambios en el Receptor GABA (Ácido γ-aminobutírico)
En insectos, el receptor GABA es un canal heteromultimérico abierto por el ión cloro, un inhibidor de canales de neurotransmisión en el sistema nervioso y las uniones neuromusculares (Bermudez et al. 1991).
El receptor GABA es el sitio de acción para ciclodienos y avermectinas al igual que para fipronil (Ffrench-Constant et al. 1993a). La resistencia está dada por el gen Rdl (Resistencia a dieldrín), el cual codifica para la subunidad RDL del receptor GABA. La sustitución Ala302Ser confiere insensibilidad al insecticida al interactuar directamente con el sitio de unión del insecticida dentro del poro del canal iónico y alostéricamente, desestabilizando la conformación preferida del insecticida, a través de un fenómeno conocido como desensibilización (FfrenchConstant et al.1998). En Drosophila se identificaron por primera vez subunidades del receptor GABA conteniendo Rdl, las cuales se han encontrado expresadas en el sistema nervioso de insectos resistentes a dieldrín, entre ellos Ae. aegypti (Thompson et al. 1993). En Drosophila simulans Sturtevant y Myzus persicae (Sulzer) (Hemiptera: Aphididae), el mismo residuo es reemplazado por glicina (Ffrench-Constant et al. 1993b).
1.2. Canales de sodio dependientes de voltaje (kdr)
Los canales de sodio dependientes de voltaje son el blanco de acción del DDT y piretroides. Estos insecticidas actúan sobre el sistema nervioso del insecto causando decaídas lentas del potencial de acción, generando la iniciación de descargas repetitivas en los axones motores y sensoriales (Soderlund y Bloomquist 1989). Estudios electrofisiológicos en Ae. aegypti y An. stephensi Liston han demostrado que estos fenómenos resultan de la modificación en la cinética de apertura de estos canales (Hemingway et al. 1989; Vatandoost et al. 1996).
El para-canal de sodio es un complejo de proteínas de más de 2000 aminoácidos, compuesto por 4 dominios homólogos separados por enlaces hidrofílicos. Cada uno de estos dominios contiene 6 a-hélices hidrofóbicas extendidas sobre la membrana (S1-S6) y cuyas secuencias contribuyen a las propiedades funcionales del canal (Loughney et al. 1989).
El gen Para, el cual codifica el canal de sodio, se clonó originalmente de D. melanogaster (Loughney et al. 1989) pero la primera mutación confiriendo resistencia, denominada “Resistencia Knockdowm” o kdr, se identificó en Musca domestica Linnaeus (Williamson et al. 1993). Los fenotipos kdr poseen una mutación puntual (Leu1014Fen) en el segmento transmembranal S6 del dominio II, la cual produce 10-30 veces resistencia a DDT y piretroides en M. domestica (Williamson et al. 1996). Esta mutación se ha identificado en insectos resistentes a piretroides pertenecientes a los órdenes Diptera (M. domestica, An. gambiae Giles), Blattodea (Blatella germanica (Linnaeus)) (Dong 1997), Lepidoptera (Plutella xylostella Linnaeus) (Schuler et al. 1998) y Hemiptera (M. persicae) (Martínez-Torres et al. 1999).
Otras mutaciones puntuales en el mismo nucleótido (Leu1014His: An. gambiae. Leu1014Ser: An. gambiae, Culex pipiens Linnaeus) también confieren resistencia a DDT y piretroides, aunque con menor frecuencia (Martínez-Torres et al. 1998; Ranson et al. 2000a).
Una sustitución adicional encontrada en cepas de M. domestica, Metionina918-Treonina, cerca al dominio IIS4-S5, en combinación con la mutación Leu1014-Fen, presenta niveles elevados de resistencia a piretroides (más de 500 veces), denominándose resistencia super-kdr (Williamson et al. 1996). Esta mutación no tiene efecto sobre la dependencia de voltaje del canal de sodio pero sí reduce la disponibilidad de los canales e incrementa la tasa de inicio y recuperación de la inactivación (Vais et al. 2001).
Martínez-Torres et al. (1998) desarrollaron una prueba diagnóstica basada en la amplificación por PCR de alelos específicos, la cual permite discriminar entre individuos homocigóticos susceptibles, homocigóticos resistentes y heterocigóticos con la mutación Leu1014Fen. Debido a que el fenotipo kdr es semi o totalmente recesivo (Paton et al. 2000), con genes de resistencia en bajas frecuencias, la capacidad de identificar heterocigóticos es importante en la detección temprana y manejo de la resistencia en el campo. Esta prueba diagnóstica ha sido modificada por Ranson et al. (2000a) para identificar la mutación Leu1014Ser en An. gambiae.
En Drosophila se ha usado un enfoque diferente para aislar mutantes tipo kdr utilizando un método basado en el fenotipo de sensibilidad a la temperatura. De esta forma se han identificado dos clases de mutaciones ubicadas en posiciones equivalentes a las mutaciones kdr y super-kdr pero hasta la fecha no se ha establecido su papel en el desarrollo de resistencia (Ffrench-Constant et al. 1998).
1.3. Acetilcolinesterasas (AchE)
La acetilcolinesterasa es una enzima clave en el sistema nervioso al catalizar la hidrólisis del neurotransmisor Acetilcolina sobre las membranas de los nervios post-sinápticos. En insectos, la forma molecular predominante es un dímero anfifílico globular anclado en la membrana mediante un glicolípido (Vontas et al. 2002). AchE es el principal blanco para organofosforados y carbamatos, los cuales inhiben la actividad enzimática mediante fosforilación covalente o carbamilatando el residuo de serina dentro del sitio activo (Corbett 1974).
La resistencia a insecticidas mediada por AchE está relacionada con cambios cualitativos y cuantitativos en la enzima y con mutaciones puntuales generalmente acompañadas por modificación de los parámetros cinéticos de la hidrólisis de acetilcolina. Tales mutaciones involucran sustituciones de aminoácidos en el sitio activo de la enzima (Walsh et al. 2001).
En general, los niveles de insensibilidad a insecticidas conferidos por cada sustitución individual son bajos pero en combinación producen enzimas altamente resistentes. El alto número de mutaciones puntuales en AchE contrasta con las pocas mutaciones responsables para resistencia fuerte, encontradas en otros sitios blancos alterados (GABA o kdr). Este número elevado de mutaciones presentes en AchE se atribuye a la comunalidad sustrato-análogo insecticida y los receptores de acetilcolina (Vontas et al. 2002). Se han registrado mutaciones específicas en AchE que confieren resistencia en D. melanogaster Meigen (Mutero et al. 1994) y M. domestica (Walsh et al. 2001).
En Cx. pipiens existen mínimo dos genes, AchE1 y AchE2, los cuales se diferencian en su especificidad de sustrato, sensibilidad y patrones de migración electroforética (Malcolm et al. 1998). AchE2 es ligado al sexo pero aun no ha sido asociado con resistencia. En Ae. aegypti y An. stephensi, también se han identificado genes AchE aunque son pocas las referencias de mecanismos de resistencia basados en AchE en estas especies (Vaughan et al. 1998). Estos genes también están ligados al sexo. Esto sugiere que los genes clonados a partir de estos mosquitos no representan el sitio blanco del insecticida o por el contrario, si existe la resistencia basada en AchE alterada, ésta debe estar ligada al sexo en estas especies (Hemingway y Ranson 2000).
En Drosophila se han identificado cinco mutaciones puntuales dentro del gen AchE asociadas con resistencia a organofosforados y carbamatos (Mutero et al. 1994). Estas mutaciones también se han identificado mediante estudios de mutagénesis sitio-dirigida en el gen AchE de Ae. aegypti (Milatovic et al. 1997), pero ninguna de ellas se ha identificado en cepas coleccionadas en el campo o seleccionadas en el laboratorio.
2. Incremento en la tasa de detoxificación de los insecticidas
En el metabolismo de los insecticidas se involucran principalmente tres familias enzimáticas: carboxilesterasas, glutation S-transferasas (GST) y mono-oxigenasas. La actividad de una o más de estas enzimas a menudo es elevada en poblaciones de insectos resistentes, pero en contraste con la resistencia dada por alteraciones en el sitio blanco, no se conocen totalmente los mecanismos moleculares de esta resistencia metabólica. La identificación de enzimas involucradas en la resistencia a insecticidas se complica además por la complejidad de tales familias enzimáticas y las dificultades para identificar genes ortólogos entre diferentes especies de insectos (Ranson et al. 2002a).
2.1. Carboxil-esterasas
Estas enzimas catalizan la hidrólisis de ésteres carboxílicos y se han asociado como primer mecanismo de resistencia a organofosforados, carbamatos y en menor proporción a piretroides (Hemingway y Karunaratne 1998). Se han encontrado niveles elevados de esterasas inespecíficas en el 90% de los casos de tolerancia a insecticidas y en más de 30 especies de insectos resistentes (Hemingway et al. 2000).
Las esterasas comprenden seis familias proteicas pertenecientes a la superfamilia α/β hidrolasas (Cygler et al. 1993). En Diptera, estas enzimas son codificadas por un grupo de genes sobre el mismo cromosoma (Cr. 3R), donde cada uno de sus miembros puede sufrir modificaciones que confieren resistencia. Tales modificaciones pueden ser cambios aminoacídicos que alteren la especificidad del sustrato (encontrado en An. arabiensis Patton, An. stephensi, An. culicifacies Giles), presencia de múltiples copias génicas amplificadas en insectos resistentes (Cx. quinquefasciatus Say, Cx. tarsalis Coquillett, Cx. pipiens, Cx. tritaeniorhynchus Giles), mutaciones puntuales (An. arabiensis, An. culicifacies, An. stephensi) o sobreproducción constitutiva (An. albimanus, An. culicifacies, Cx. quinquefasciatus, Cx. tarsalis) (Hemingway y Ranson 2000).
Bioquímicamente, las esterasas actúan uniéndose rápidamente al insecticida pero liberando lentamente los metabolitos de éste, es decir, secuestrando el insecticida antes que llegue a su sitio de acción. Lo anterior requiere altas cantidades de estas enzimas debido a la estequiometría de la reacción, desencadenando la sobreproducción enzimática y por ende el desarrollo de resistencia (Karunaratne et al. 1993). Molecularmente, el mecanismo más común de resistencia mediado por esterasas es la co-amplificación de los genes esta2¹ y estβ2¹, los cuales presentan distribución mundial y cuya base bioquímica y molecular de resistencia ha sido bien caracterizada en el mosquito Cx. quinquefasciatus (Vaughan et al. 1997).
La alta homología entre los genes esta y estβ sugiere que éstos han surgido como resultado de un evento ancestral de duplicación génica (Raymond et al. 1991). Los genes esta2¹ y estβ2¹ se encuentran en el mismo amplicón alejados 2.7 kb en insectos resistentes y solo 1.7 kb en insectos susceptibles. La diferencia está dada por la presencia de tres inserciones en el espacio intergénico amplificado (Vaughan et al. 1997). Las inserciones pueden haber introducido elementos reguladores adicionales (Hemingway et al. 1998).
Recientemente se ha descrito co-amplificación de esta2¹ y estβ2¹ ligada a un tercer gen, aldehído oxidasa, el cual a su vez se encuentra co-elevado dentro del mismo amplicón con tales alelos pero no con otros genotipos de esterasas (Hemingway et al. 2000).
El análisis de fragmentos de restricción y homología de secuencias en cepas de insectos resistentes procedentes de distintos continentes, ha permitido confirmar que la co-amplificación de esta2¹ y estβ2¹, posee un origen único y se ha propagado mundialmente (Hemingway y Karunaratne 1998; Raymond et al. 1998). Esta rápida e inesperada migración de insectos resistentes sugiere una gran ventaja en la eficacia biológica de los portadores de este amplicón en presencia del insecticida (Hemingway y Karunaratne 1998), resultando en serias implicaciones para el control del vector y la enfermedad.
Otros fenotipos de resistencia más variables y menos comunes involucran coamplificación de esta3 y estβl, o amplificación individual de estβl, o estal y esta5¹, los cuales presentan distribución geográfica restringida (Guillemaud et al. 1997; Severini et al 1997; Vaughan et al. 1997). La región cromosómica que contiene estos genes de esterasas, presumiblemente representa un punto susceptible de amplificación, una teoría sustentada por la amplificación de genes esterasa β homólogos en Cx. tritaeniorhyncus (Karunaratne et al. 1998).
2.2. Glutation-S-transferasas
La enzima Glutation S-transferasa (GST) pertenece a una gran familia de isoenzimas multifuncionales involucradas en el metabolismo, detoxificación y excreción de un amplio rango de xenobióticos incluyendo los insecticidas. Ellas se encargan de proteger a las células del estrés oxidativo y de los tóxicos químicos, catalizando la conjugación de los componentes electrofílicos con el grupo tiol de la glutatión reducida (GSH), obteniendo productos más hidrosolubles y de mayor excreción (Salinas y Wong 1999).
En eucariontes se han identificado más de 40 genes GST clasificados en 13 grupos según la identidad de sus secuencias, propiedades inmunológicas y en algunos casos, especificidad de sustrato (Sheehan et al. 2001). En insectos se han reconocido solo tres clases: Delta, Sigma y Epsilon (Ranson et al. 2001), las cuales están potencialmente relacionadas con el desarrollo de resistencia a insecticidas.
GST se asocia principalmente con resistencia a DDT (catalizando la dehidroclorinación del DDT a su metabolito menos tóxico DDE) (Clark y Shamaan 1984), organofosforados y recientemente piretroides (Kostaropoulos et al. 2001; Vontas et al. 2001), a través de mecanismos de cambio en la especificidad del sustrato (An. gambiae), niveles elevados de actividad (An. gambiae, An. dirus Peyton & Harrison, An. stephensi, An. subpictus Grassi, An. culicifacies y Aedes aegypti) y regulación génica (con posible amplificación) (An. gambiae, An. dirus y Ae. aegypti), aunque los elementos reguladores que controlan la expresión de GST no se han identificado aún (Hemingway y Ranson 2000).
GST de la clase Delta son codificadas por una familia multigénica. En D. melanogaster y An. gambiae tal familia se encuentra agrupada (Toung et al. 1993; Ranson et al. 1998), en contraste con M. domestica, donde estos genes se encuentran dispersos a través de todo el genoma (Zhou y Syvanen 1997). Los genes de esta subfamilia han sido localizados sobre el cromosoma 2R, división 18B y 19D y se expresan en niveles elevados tanto en larvas como adultos de An. gambiae (Ranson et al. 1998; Ranson et al. 2001). La familia GST de la clase Sigma consiste de un único gen en todas las tres especies (Beall et al. 1992; Reiss y James 1993). Se ha observado que la resistencia a DDT en An. gambiae es diferencial dependiendo del estadio de su ciclo de vida; así, el gen GSTs1 se expresa en larvas pero su detección es escasa en insectos adultos, estadio responsable de la transmisión de malaria (Reiss y James 1993).
Recientemente se ha descrito GST clase Epsilon en An. gambiae y se sugiere que representa la mayor familia enzimática confiriendo resistencia a DDT en este vector. Se han identificado dos genes codificando enzimas funcionales GSTe1 y GSTe2. Uno de estos genes, GSTe2, presenta actividad dehidroclorinasa y niveles de sobre-expresión cinco veces mayores en cepas resistentes que en cepas susceptibles (Ranson et al. 2001). Estos genes se ubican en la división 33B sobre el cromosoma 3R que contiene uno de los dos mayores loci (rtd1) para rasgos cuantitativos asociados con resistencia a DDT (Ranson et al. 2000b). Ranson et al. (2001) propusieron que rtd1 podría ser un elemento regulador actuando en Cis, el cual estaría controlando la expresión de los genes GST clase Epsilon. Si múltiples miembros de esta familia génica están bajo el control de un factor regulador común, una mutación en este factor podría explicar la elevada actividad de GST observada en ensayos bioquímicos (Ding et al. 2003).
Un estudio sobre las propiedades bioquímicas e inmunológicas de la subfamilia Epsilon identificó un alelo GSTe1K, el cual presentó altos niveles de actividad peroxidasa (Ortelli et al. 2003). En Nilaparvata lugens Stal (Hemiptera: Delphacidae) se ha demostrado que la actividad de peroxidasa protege contra daños causados por productos de la peroxidación lipídica inducidos por la exposición a piretroides (Vontas et al. 2001). Aunque este mecanismo no se ha identificado en mosquitos, es posible que insectos portadores de este alelo posean ventajas en su eficacia biológica en presencia de insecticidas (Ortelli et al. 2003).
2.3. Citocromos P450
Los citocromos P450 son una superfamilia de hemoproteínas responsables del metabolismo oxidativo de una amplia variedad de componentes exógenos (aleloquímicos vegetales, promutágenos e insecticidas) y endógenos (hormonas juveniles, ecdiesteroides, feromonas) del metabolismo (Scott y Wen 2001). P450 han sido encontrados en todos los sistemas vivos y en un rango diverso de especies de insectos, incluyendo Diptera (Scott 1999), Lepidoptera (Rose et al.1997) y Coleoptera (Sharf et al. 2001).
Se ha identificado resistencia mediada por P450 para casi todas las clases de insecticidas, principalmente piretroides (Berge et al.1998), organoclorados y reguladores de crecimiento (Brogdon y McAllister 1998a). Se proponen dos posibles mecanismos genéticos: (1) Cambios estructurales en P450s específicos o (2) Niveles elevados de expresión de P450s. Mutaciones puntuales dentro de genes estructurales P450 pueden resultar en actividades catalíticas incrementadas o alta afinidad por el insecticida (Scott y Wen 2001). Algunos estudios han registrado sobre-expresión constitutiva (CYP6G1, CYP12D1) e inducción post exposición a DDT (CYP12D1) en cepas de insectos resistentes (Brandt et al. 2002), pero en pocos casos se ha establecido conexión definitiva entre la expresión elevada de un gen P450 específico y el desarrollo de resistencia.
En D. melanogaster se han aislado 83 genes putativos para codificar P450s funcionales. Estos han sido clasificados en 25 familias, pero más del 50% pertenece a las familias CYP4 o CYP6 (Tijet et al. 2001). Recientemente, Daborn et al. (2002) utilizando análisis de microarreglos sobre todos los P450s de D. melanogaster demostraron que DDT-R, un gen que confiere resistencia a DDT, está asociado con un incremento en la transcripción del gen Cyp6g1. Esto se confirmó mediante análisis transgénicos de Cyp6g1, los cuales demostraron que la transcripción es necesaria y suficiente para el desarrollo de resistencia.
En An. albimanus se identificaron 17 genes que codifican proteínas de las familias CYP4 y CYP9. En An. gambiae se identificaron 34 genes P450: 14 genes pertenecientes a la familia CYP6, 18 genes para CYP4 y 2 para CYP9. Estos genes se localizan en el cromosoma 3R, división 30A (CYP6), cromosoma 2R, división 13C (CYP6P) y división 12C (CYP4H) (Ranson et al. 2002b). Lo anterior se relaciona con la identificación de dos loci de resistencia para permetrina, uno de los cuales se localiza en el cromosoma 3R, división 30 (Ranson et al. 2002b). La co-localización de este loci de resistencia con un grupo de genes P450, plantea el papel de una o más de estas proteínas en conferir resistencia a piretroides en An. gambiae.
2.4. Aldehído Oxidasa
En vertebrados superiores, la enzima aldehído oxidasa está involucrada en el metabolismo oxidativo de xenobióticos y en la reducción de nitrosaminas, ácidos hidroxámicos, N-óxidos, hidrocarbonos aromáticos nitropolicíclicos, colorantes azo y sulfóxidos (Calzi et al. 1995), pero existen pocos estudios sobre su papel en el metabolismo de los insectos.
Esta enzima pertenece al grupo de hidrolasas que contienen Molibdeno. Se asume que para todas las enzimas de este grupo, los sustratos actúan en el molibdeno central, reduciéndolo del estado Mo(VI) a Mo(IV). Posteriormente, los equivalentes reductores son transferidos vía centros de sulfuro de hierro y la enzima es re-oxidada por interacción con el oxígeno (Turner et al. 1995).
Esta enzima se describió por primera vez para insectos en la cepa PELRR resistente de Cx. quinquefasciatus (Hemingway et al. 2000). El gen que codifica esta enzima fue identificado en ligamiento con el gen esta, dentro del amplicón de 30 kb asociado con resistencia a insecticidas el cual contiene los genes esta2’ y estβ2¹. Lo anterior coincide fuertemente con estudios previos de mapeo genético en An. albimanus (Narang y Seawright 1983) y sugiere una ventaja selectiva de los individuos portadores de este amplicón con respecto a los amplicones que contienen otras esterasas (Coleman et al. 2002).
Coleman et al. (2002), mediante análisis de secuenciamiento y clonación, identificaron para aldehído oxidasa una secuencia de 1266 aminoácidos, la cual transcribe una proteína de 150 kDa. Análisis por RT-PCR en cepas susceptibles y resistentes sugieren que el gen amplificado es transcrito en todas las fases del ciclo de vida de los mosquitos, presentando mayor actividad en larvas resistentes, con un pico en los estadios 3 y 4, disminuyendo progresivamente en pupas y adultos.
Aunque el papel específico del gen aldehído oxidasa en la resistencia a insecticidas no se ha determinado totalmente, se ha demostrado que insecticidas como el paration y herbicidas conteniendo el grupo aldehído son reconocidos como sustratos o inhibidores enzimáticos (Hemingway et al. 2000). Trabajos realizados en mamíferos han involucrado esta enzima en el desarrollo del sistema nervioso central, uno de los principales blancos de acción de los insecticidas (Calzi et al. 1995), lo cual es otra evidencia de su posible papel en la resistencia a insecticidas.
Resistencia Cruzada
La resistencia cruzada implica el mismo mecanismo de resistencia para dos clases de insecticidas no relacionados (Najera y Zaim 2002). Este tipo de resistencia se presenta principalmente entre piretroides y DDT en diferentes especies de insectos. Registros de resistencia tipo kdr en An. gambiae en África oriental postulan que la resistencia ha sido seleccionada por el uso temprano de DDT y/o el uso agrícola de piretroides (Chandre et al. 1999). La resistencia cruzada es específica de producto más no del tipo de insecticida, lo cual se ha demostrado en An. stephensi donde la resistencia a permetrina no confiere resistencia cruzada a deltametrina en larvas y adultos pero sí a otros cianopiretroides (Curtis y Townson 1998) y Etofenprox (Curtis 1993). Recientemente se ha registrado resistencia cruzada tipo kdr en Ae. aegypti (Brengues et al. 2003). La presencia de resistencia cruzada tipo kdr entre DDT y piretroides amenaza el uso de piretroides tanto en rociamientos intradomiciliares como en toldillos impregnados para el control de malaria.
Un estudio realizado en An. funestus Giles demostró elevados niveles de resistencia a piretroides pero no a DDT (Hargreaves et al. 2000). Estas evidencias han motivado la idea de restaurar los programas de rociamiento con DDT en países como Madagascar y en la provincia de Kwazulu/Natal en Sur África, en áreas donde se advierte alta transmisión de malaria (Brooke et al. 2001). El impacto del uso reciente de DDT ha sido asociado con una reducción del 60% de los casos de malaria durante el 2001 en Sur África (Curtis 2002).
Detección y Vigilancia de la Resistencia
La capacidad de prevenir o retardar la evolución del desarrollo de resistencia a insecticidas se fundamenta en la implementación de estrategias para el manejo y vigilancia de la resistencia. Tres aspectos importantes en el diseño de tales estrategias son (1) el establecimiento de líneas-base de susceptibilidad, (2) la identificación de los mecanismos de resistencia y (3) el uso de métodos que vigilen las frecuencias de resistencia y el efecto de las estrategias de control (Brogdon y McAllister 1998a).
La identificación de los mecanismos de resistencia determina el espectro de resistencia cruzada, facilita la escogencia de insecticidas alternativos y permite el mapeo detallado de áreas con poblaciones resistentes. Los bioensayos o pruebas biológicas tienen la capacidad de encontrar casos de resistencia producidos por cualquiera de los diferentes mecanismos bioquímicos o neurofisiológicos. La OMS (WHO 1981) implementó el uso de papeles impregnados con insecticidas o sinergistas en dosis estandarizadas, basados en la correlación entre mortalidad vs tiempo de exposición y mortalidad vs dosis letales. Otra alternativa para la realización de los bioensayos es el uso de botellas de vidrio impregnadas con insecticidas la cual ha sido estandarizada por el Centro para el Control y Prevención de Enfermedades en Estados Unidos (CDC). Esta aproximación simplifica el procedimiento de los bioensayos convencionales e incrementa la cantidad de información que puede obtenerse de un grupo limitado de mosquitos (Brogdon y McAllister 1998b).
Debido a que los piretroides causan inducción de parálisis temporal, más conocida como “knockdown”, se ha asociado la resistencia a piretroides con un incremento significativo en el tiempo de noqueo antes de disminuir la mortalidad, por lo que dicho tiempo es un buen indicador para la detección temprana de resistencia a piretroides (WHO 1992) y puede incluirse en los programas de vigilancia de resistencia a estos insecticidas al aportar información inicial acerca de la resistencia basada en el gen kdr (Chandre et al. 1999).
Los métodos bioquímicos y moleculares pueden identificar mecanismos específicos de resistencia y detectar genes de resistencia cuando éstos aun estén en bajas frecuencias y utilizando un número mínimo de insectos (Brogdon 1984). Las pruebas bioquímicas están disponibles para la evaluación de esterasas inespecíficas, oxidasas de función mixta, glutation S-transferasas y acetilcolinesterasas inhibidas, las cuales pueden ser detectadas en un mismo individuo. Aunque las pruebas están inicialmente diseñadas para realizarse en condiciones de laboratorio, pueden estandarizarse bajo condiciones de campo directamente en las áreas de vigilancia.
Actualmente se dispone de estudios comparativos de la estructura y función de los genomas totales de An. gambiae y D. melanogaster (Ranson et al. 2000b). Estos análisis permitirán descubrir nuevas moléculas hormonales, neuronales y reguladoras que puedan utilizarse como blancos para el desarrollo de nuevas clases de insecticidas; Igualmente, los avances recientes en genómica funcional permitirán determinar los cambios moleculares precisos que resulten en fenotipos de resistencia, contribuyendo así al manejo de la resistencia en las poblaciones de campo (Hemingway et al. 2002).
Para el manejo de la resistencia se están desarrollando numerosas herramientas, desde nuevos insecticidas químicos hasta mosquitos transgénicos. Se han considerado también distintas estrategias, entre ellas el uso de mezclas de insecticidas con diferentes modos de acción (Corbel et al. 2002), las cuales deben producirse industrialmente. Entre las estrategias más comunes se encuentran la aplicación de insecticidas en mosaico y rotaciones. La aplicación en mosaico consiste en dividir el área a tratar en zonas, seleccionar dos insecticidas de resistencia no cruzada y aplicar en cada zona uno de éstos (Ej., alternando piretroides y organofosforados). En la estrategia de rotación se aplica un insecticida en un ciclo y otro, que no sea de resistencia cruzada, en el ciclo siguiente. (Por Ej., piretroides – organofosforados /carbamatos) (Penilla et al. 1998).
Se han desarrollado modelos matemáticos y simulaciones in vitro de la evolución de los genes de resistencia asociados a diferentes patrones de usos de los insecticidas (Tabashnik 1990), pero estos modelos no han sido aplicados en estudios de campo dada la dificultad práctica de estimar correctamente los cambios en las frecuencias de los genes de resistencia en los programas de control químico aplicados en gran escala (Penilla et al. 1998; Hemingway y Ranson 2000).
Conclusiones
Todos los insecticidas químicos ejercen, en mayor o menor extensión, presiones selectivas sobre las poblaciones de insectos que intentan controlar; por lo cual, en un tiempo las poblaciones resistentes comienzan a emerger. El tiempo necesario para el desarrollo de resistencia depende de numerosos factores incluyendo la frecuencia y naturaleza de los genes de resistencia, las estrategias para su manejo, las dosis y frecuencias de aplicación de los insecticidas y la eficacia biológica de las poblaciones resistentes en relación con las susceptibles. Mientras no haya alternativas efectivas al uso del control químico, éste debe enmarcarse en programas de control integrado, adaptándose a las condiciones locales con énfasis en la rotación de insecticidas a fin de prevenir, retardar o revertir el desarrollo futuro de resistencia en las poblaciones de insectos vectores. Es indispensable en los programas de control de las enfermedades transmitidas por vectores el uso de métodos que vigilen las frecuencias de resistencia y el efecto de las estrategias de control. Todas las decisiones sobre el uso de insecticidas deben tomarse considerando los componentes del manejo de la resistencia y el impacto mínimo sobre los humanos, los organismos no blanco y el ambiente.
