Abstract
The life cycle of the orb-weaving spider
Introducción
Esta especie se reconoce por exhibir un marcado polimorfismo cromático, que va de amarillo claro hasta naranja rojizo. El caparazón es de color amarillo y presenta una marca longitudinal oscura sobre la parte media, el abdomen es ovalado terminado en forma aguda, sobre el dorso se observa una serie de manchas blancas y negras; en el vientre se distingue una mancha oscura entre el surco epigástrico y los espineretes. El abdomen de los machos es más delgado y corto que el de las hembras pero el patrón de coloración es similar; construyen telas orbiculares verticales y exhiben hábitos diurnos a la espera de las presas, constituidas principalmente por insectos voladores y saltadores; en ocasiones aprovechan cualquier tipo de sustrato para construir sus telas, incluyendo objetos fabricados por el hombre como recipientes de deshecho y postes de cercas.
Hasta la fecha sólo tres estudios sobre ciclos de vida de arañas se han realizado en Colombia: el de
Teniendo en cuenta que la araña
Materiales y Métodos
El presente estudio se llevó a cabo en inmediaciones del "Arboretum Francisco Bayón" del Instituto de Ciencias Naturales de la Universidad Nacional de Colombia, sede Bogotá, a lo largo de 10 meses (mayo/2000-febrero/2001). El ciclo de vida y algunas características reproductivas de
Los individuos se confinaron en jaulas de malla y cámaras de cría. Las jaulas y las cámaras se mantuvieron en un invernadero (Fig. 1) con techo plástico y encerrado con malla de alambre (diámetro de ojo: 3 cm). Las jaulas, elaboradas con malla de anjeo plástico, tuvieron unas dimensiones de 0.40 m x 0.40 m x 0.70 m; en la parte frontal se ubicó una abertura de manga para facilitar el suministro de las presas (Fig. 2). Las jaulas se montaron sobre materos plásticos de 1.2 m x 0.4 m x 0.5 m provistos con tierra sobre la cual se sembró pasto kikuyo. Adicionalmente se utilizaron recipientes plásticos cilíndricos de dos tamaños como cámaras de cría. Unos de 26 cm de alto x 15 cm de diámetro, para alojar parejas y hembras capturadas después de la cópula, cuya apertura superior se cubrió con muselina (Fig. 3a). Otros, de 6.5 cm de alto x 2.1 cm de diámetro, con tapón de espuma, para alojar los juveniles nacidos en cautiverio (Fig. 3b). En ambos casos el fondo de los recipientes se recubrió con arena para mantener la humedad y permitir enterrar pequeñas estructuras que sirvieran de soporte para la construcción de las telas. Todos los individuos se alimentaron semanalmente con insectos, principalmente dípteros, que se colectaron en pastizales de los alrededores del arboretum.

Invernadero empleado para el confinamiento y cría de la araña A. variabilis.

Jaula de cría para el confinamiento de A. variabilis.

Cámaras empleadas para la cría de A. variabilis. a. Para parejas. b. Para juveniles.
Periódicamente las cámaras de cría se revisaron para detectar las mudas. Simultáneamente, los individuos de diferentes tamaños colectados en Tocancipá y Mosquera y las mudas, se midieron con el fin de estimar el número de ínstares necesarios para alcanzar el estado adulto. En 1912, Przibram y Megusâr (citado por Francke y Sissom 1984) propusieron una ley de crecimiento en la cual se asume que el aumento en la medida de cierta estructura está dado por un valor constante durante las diferentes etapas de incremento de tamaño o mudas, esta ley fue utilizada para estimar el número de mudas que necesita un individuo de
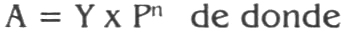

donde A es la medida de una estructura en el adulto, Y es la medida de la misma estructura en un juvenil de ínstar conocido, P es el factor de progresión (1,26 según Przibram y Megusâr) y n es el número de mudas requeridas para que el espécimen juvenil alcance el tamaño del adulto.
Las estructuras morfológicas consideradas para dichas mediciones fueron el ancho del caparazón (placa dorsal que recubre el cefalotórax) y la longitud del fémur I; éstas se tomaron empleando un estereoscopio Stemi SV marca Zeizz, dotado con una reglilla micrométrica.
Resultados y Discusión
Las observaciones realizadas para determinar el ciclo de vida de
Cópula
El proceso de cópula se observó en condiciones naturales y de laboratorio; se inicia cuando uno o varios machos se ubican en la periferia de la tela de una hembra, tendiendo un hilo que adhieren a dicha tela (hilo de cópula), por el cual transmiten vibraciones a la hembra residente golpeando con sus patas delanteras para anunciar su presencia; en caso de ser receptiva ésta se acerca hacia el macho y después de una serie de toques con sus patas anteriores, decide aceptar o rechazar al macho. Los patrones generales de la secuencia de apareamiento de
Adicionalmente, se detectó en campo que una misma hembra podía copular con varios machos en un mismo período de apareamiento, lo cual no implica que la hembra realice varias posturas, pues de acuerdo con lo observado en laboratorio las hembras de
En varias ocasiones se detectaron machos adultos en proximidades de telas de hembras subadultas; Eberhard (com. pers.) sugiere que el macho que ha copulado con una hembra virgen tiende a tener cierta ventaja sobre el resto (mayor número de huevos fecundados por sus espermatozoides), sin embargo Robinson (1982) señala al respecto, que los machos prefieren copular con hembras recién mudadas porque en este estado se encuentran imposibilitadas para alimentarse reduciendo así la posibilidad de ser depredados.
Inmediatamente después de la cópula, el macho se deja caer para evitar ser atrapado y consumido por la hembra; este comportamiento además le garantiza la posibilidad de volver a copular de nuevo con la misma o con otra hembra. A lo largo de este estudio sólo tres eventos de canibalismo se registraron.
Después de la cópula, las hembras de
Duración de los diferentes estadíos del ciclo de vida de
Los datos en paréntesis indican el tiempo acumulado en días.
** No se pudo calcular D.S., por contarse con un solo dato.
C= Cópula; P= Postura; E= Eclosión;
I-VII= Ínstares; M= Machos; H= Hembras.
Postura
El proceso de postura se inicia en horas de la madrugada con la construcción de un capullo de seda amarilla, que consta de un disco basal sobre el cual los huevos son depositados y posteriormente recubiertos por una densa malla de hilos entretejidos (Fig. 4), esta estructura es rodeada por una malla menos densa, que finalmente es adherida al substrato (hojas de kikuyo
A partir de las observaciones de hembras grávidas, confinadas en las cámaras de cría, se estableció que éstas entran en un período de actividad baja dos días antes de la postura (no construyen telas, ni se alimentan). Después de la oviposición, la hembra se ubica por dos o tres días sobre el saco de huevos y posteriormente los abandona para construir su tela en otro lugar.
El saco de huevos de
De los 10 sacos de huevos observados (Tabla 2), cuatro se colectaron en campo y seis en el laboratorio. Los huevos son translúcidos, de color crema claro y están unidos entre sí por medio de una sustancia transparente (Nentwig y Heimer 1987), la masa de huevos presenta una disposición más o menos esférica. El número de huevos por postura fue muy variable encontrándose en un rango entre 28 y 123 huevos/ovisaco; el promedio de huevos por ovisaco fue de 76.5 ± 34.9 y el porcentaje de eclosión de 32.8.
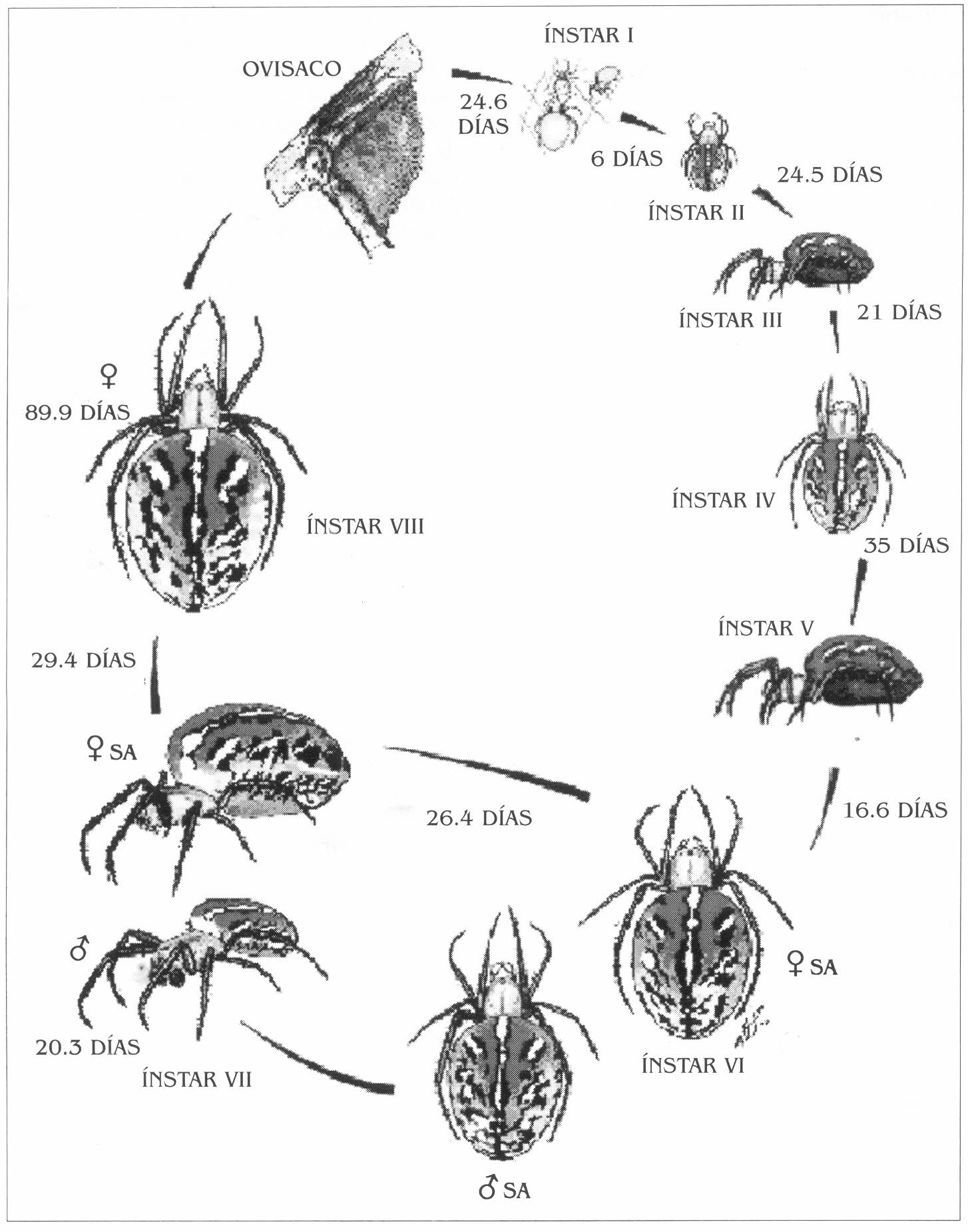
Ciclo de vida de la araña
Número de huevos por ovisaco de
Sacos colectados en campo.
El bajo porcentaje de eclosión en ovisacos de
Al efectuar un cálculo posterior del porcentaje de eclosión, sin tener en cuenta estos cuatro ovisacos, arrojó un valor de 60.5%. Esta misma situación se presenta en
En la literatura han sido registrados diferentes datos de posturas; a continuación se reseñan algunos de ellos de manera sucinta. Para
Basados en los datos anteriores se evidencia que
El tiempo de eclosión observado para
Desarrollo post-embrionario
Una vez eclosionados los huevos de
Los individuos de
Al cuarto día, su actividad aumenta y la coloración es mucho más definida, los ojos están completamente pigmentados, al igual que los segmentos distales de las patas y se observan vestigios de manchas oscuras en el dorso del opistosoma.
Las arañas mudan por primera vez marcando el inicio del ínstar II y salen del saco de huevos. Su coloración es más amarilla y las manchas oscuras del opistosoma ya son evidentes (Fig. 4), empezándose a observar unas pequeñas manchas blancas sobre el mismo. La duración de este ínstar es de tres a cuatro semanas (3.5 ± 0.7) (Tabla 1).
A partir de este momento las arañas juveniles se alimentan por sí solas y son capaces de construir pequeñas telas orbiculares. En el campo se pueden observar áreas relativamente pequeñas densamente pobladas por arañas pertenecientes a este ínstar, lo cual puede traducirse en una tasa de dispersión muy baja a esta edad.
En la segunda muda la araña consume la exuvia, esto solamente pudo ser comprobado una vez, pero al parecer es un hecho generalizado pues en ninguna cámara de cría se encontró la exuvia; por tal razón la duración del ínstar III está basada en una sola observación (21 días) (Tabla 1).
No se sabe si este evento sucede en condiciones naturales, si no es así, puede ser debido a cambios comportamentales ocasionados por el cautiverio al que fueron sometidas. Este hecho no sucede con exuvias de mudas posteriores, posiblemente debido a encontrarse más esclerotizadas y dificultar su consumo. Probablemente se trate de un hábito peculiar que no ha sido registrado en la literatura.
Los ínstares IV-VII tuvieron una duración aproximada de 27 días cada uno (Tabla 1); a partir del ínstar IV se empieza a observar un leve engrosamiento del tarso de los palpos en algunos individuos, lo cual permite desde este momento diferenciar machos de hembras; dicho engrosamiento se hace más evidente a medida que el individuo continúa con el proceso de muda. Por otro lado, entre los ínstares V y VI se comienza a notar el abultamiento de la placa genital en las hembras.
En el ínstar VII, el epiginio de la mayoría de las hembras subadultas aumenta de tamaño pero no muestra ningún rasgo de esclerotización, aunque unas pocas alcanzan la madurez sexual en este ínstar al igual que la mayoría de los machos. El tiempo de duración de este ínstar en cautiverio varió entre 14 y 42 días (4.4 ± 1.0) para aquellos individuos que no alcanzaron el estado adulto en este tiempo; el resto de individuos que no alcanzaron el estado adulto en el ínstar VII lo alcanzaron en el VIII.
En el último ínstar (VIII) se encuentran los machos y hembras que alcanzaron la madurez sexual (Fig. 4) y comprende el tiempo entre la última muda y la muerte del individuo, incluyendo aquellos que maduraron en el ínstar VII. El tiempo de vida de las hembras adultas fluctuó entre 49 y 140 días (89.9 ± 39.7) y el de los machos, entre 7 y 28 días (20.3 ± 14.2); como puede observarse, las diferencias en la duración de este período entre hembras y machos es muy variable, posiblemente esto se debió a efectos ocasionados por el cautiverio pues varios individuos murieron al momento de la muda o en los días subsiguientes. Es probable que estas muertes no fueron naturales sino inducidas por condiciones extremas de temperatura y humedad dentro de las cámaras de cría, ya que estos eventos se presentaron en días calurosos y noches muy frías.
La longevidad de las hembras parece ser mayor que la de los machos, pues se observó que la sobrevivencia de éstos no superó los 184 días, mientras que para ese mismo lapso de tiempo las hembras exhibieron una mortalidad de tan sólo 23%.
A partir de los resultados obtenidos en laboratorio, se estableció que el tiempo promedio de vida de
Los ciclos de vida varían considerablemente entre diferentes especies de arañas, así por ejemplo, Dossman et al. (1997) registran para
Se detectó, a partir de los datos obtenidos en laboratorio, que el número de ínstares requeridos para alcanzar la madurez sexual en
La variación observada en el número de mudas y tiempo de desarrollo para alcanzar la madurez sexual (Tabla 1) puede deberse en parte a la cantidad (Jacob y Dingle, 1990) y calidad de alimento (Totft, 1999) proporcionado a los individuos de
Varios autores han documentado que los machos alcanzan la madurez sexual antes que las hembras, mudando una o dos veces menos, aunque esto no es generalizado (Kaston 1978; Merrett 1988; Foelix 1996; Schneider 1997; Avilés y Salazar 1999; González et al. 1999). Al parecer esto le permite a los machos asegurar la cópula con hembras vírgenes, es decir, recién mudadas al estado adulto (Jacob y Dingle 1990; (Jakson 1980; Vollrath 1980; Austad 1982 y Christenson y Cohn 1988) citados por Bukowski y Christenson 1997; Schneider 1997). Lo anterior justifica en cierta forma que la mayoría de los machos haya madurado un ínstar antes que las hembras y además que en campo se observaran machos adultos ubicados en proximidades de telas de hembras subadultas.
En arañas el número de mudas e ínstares varía de especie a especie e incluso puede variar entre individuos de una misma especie (Foelix 1996); por ejemplo,
De acuerdo con lo anterior, se puede establecer que
Se estableció a partir de los individuos mantenidos en laboratorio, que la proporción de hembras es algo mayor que la de machos (1.13:1), aunque en campo se encontró que dicha proporción aumenta casi al doble (2.46:1), probablemente sea debido a la alta movilidad de los machos en el campo, lo cual disminuye la probabilidad de encontrarlos.
Estimación del número de ínstares
Debido a que el ciclo de vida se llevó a cabo en condiciones artificiales, posiblemente los resultados obtenidos se alejen parcialmente de los valores reales puesto que un individuo en cautiverio no puede responder de la misma manera que un individuo en condiciones naturales, ya sea por cambios microclimáticos (temperatura, humedad, luminosidad, etc.) o por cambios fisiológicos debidos en gran parte al aporte energético obtenido de una dieta que de alguna manera puede diferir de la dieta natural.
De otra parte, en condiciones naturales es prácticamente imposible establecer su ciclo de vida, pues no se pueden determinar con exactitud los tiempos y número de mudas. Con el fin de obtener otra aproximación comparativa del número de ínstares necesarios para alcanzar la madurez sexual a partir de individuos de dos ínstares conocidos colectados en campo, durante el seguimiento del ciclo de vida de
Con base en esta ley se estimó el número de ínstares para
Como se observa en la tabla 4, la nueva constante de progresión P tiene un valor de 1.3 que corresponde al promedio entre la constante calculada con las medidas del ancho del caparazón y la longitud del fémur I (1.26 y 1.34 respectivamente). Esto permite inferir que ambas estructuras crecen a una tasa diferente por lo cual es necesario promediarlas.
Número estimado de mudas de A. variabilis a partir de mediciones morfométricas.
A.C. Ancho de caparazón. L. F. Longitud del fémur I. n Número de mudas
Estimación del factor de progresión (P) a partir de datos morfométricos para A. variabilis
A.C. Ancho de caparazón. L. F. Longitud del fémur I.
P calculado a partir de n=6
Empleando el ancho del caparazón, la longitud del fémur I y la nueva constante de progresión (P= 1.3), se calculó de nuevo el número de mudas necesarias para que un individuo de ínstar II alcance el estado adulto, el resultado fue de 5.3 y 6.6 mudas, respectivamente (Tabla 3). Puesto que el proceso de muda se lleva a cabo en un solo evento; es decir, durante este proceso todas las estructuras del exoesqueleto se desprenden simultáneamente, es improbable pensar que un mismo individuo necesite un número variable de mudas para diferentes estructuras, por lo tanto es necesario promediar ambos estimados lo que da como resultado 5.9 mudas valor que debe ser aproximado a seis. Esto permite estimar que un individuo de ínstar II necesita mudar seis veces más para llegar al estado adulto.
Partiendo de lo anterior, se concluye que
Adicionalmente, se determinaron los rangos de tamaño por ínstar del ancho del caparazón y longitud del fémur I (Tabla 5), partiendo del promedio y la desviación estándar de las medidas tomadas de los individuos adultos, la constante calculada para
Debido a que los rangos de edad se calculan utilizando datos reales (las medidas de las estructuras) y datos teóricos (el factor de progresión P= 1.3) se graficó la relación del ancho del caparazón vs. longitud del fémur I medidos en individuos de diferentes edades colectados en campo (262 individuos) para comprobar si en estos rangos teóricos pueden ser ubicados dichos individuos. Como se observa en la figura 5, la mayoría de individuos (59%) tienden a agruparse dentro de un rango de edad determinado; es decir, que de acuerdo con la medida de las dos estructuras, cada uno de éstos puede ser situado en un ínstar específico. Por ejemplo, las marcas en forma de cruz (+) corresponden a individuos cuyas medidas del ancho de caparazón y largo de fémur se agrupan dentro del rango de tamaño del ínstar VII (subadultos).
A pesar de que los individuos restantes (marcas en forma de rombo) se mantienen dentro de la misma tendencia (41%), se observa que algunos pueden ubicarse en un rango de edad con respecto al ancho del caparazón y en otro con respecto a la longitud del fémur I. Esto reafirma la idea expuesta anteriormente acerca del crecimiento diferencial de estructuras en un mismo individuo. A pesar de esto, el coeficiente de regresión para las medidas de ambas estructuras (R2 = 0.9636) indica que existe una alta correlación entre las mismas, por lo cual pueden ser utilizadas en la estimación de los diferentes rangos de edad, al menos en arañas.
Rangos teóricos de tamaño de ínstar, calculados a partir del factor de progresión P = 1.3 para
A.C.: Ancho de caparazón.
L.F.: Longitud fémur I.
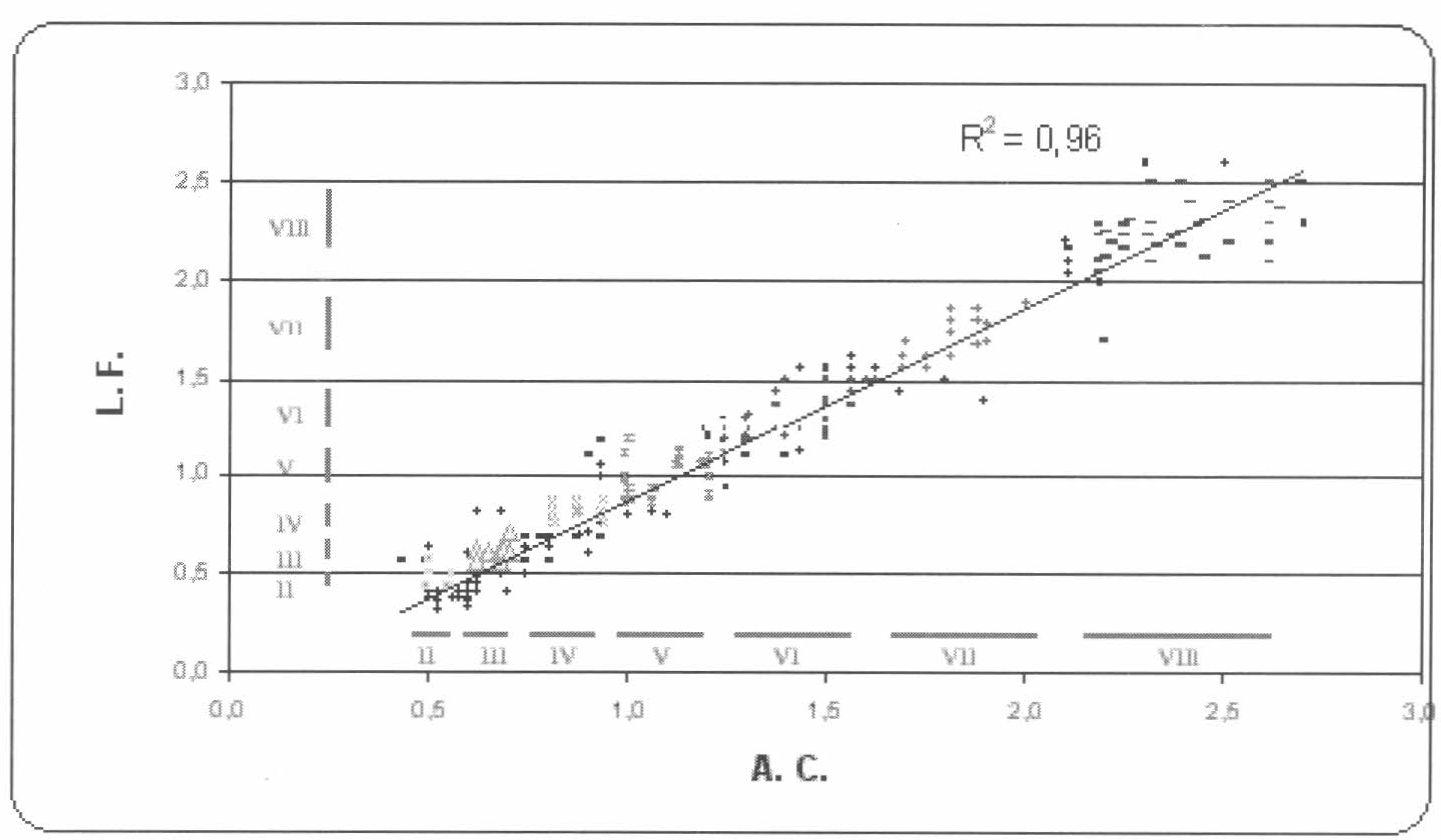
Relación ancho caparazón vs. longitud fémur I de individuos colectados en campo de diferentes edades de
Aunque al promediar y aproximar los valores de la constante y número de mudas calculados para cada estructura medida, el resultado es igual al obtenido en laboratorio, se evidencian variaciones entre el crecimiento de dichas estructuras pues cada una crece a una tasa diferente. Lo anterior sugiere que para una mayor precisión en este tipo de inferencias se requiere de la medición de un mayor número de estructuras, como podrían ser por ejemplo la longitud del caparazón, la longitud de los fémures restantes e inclusive de los otros segmentos de las patas.
Enemigos naturales de A. variabilis
A partir de las observaciones de campo se estableció que esta araña es parasitada por
Conclusiones
El ciclo de vida de la araña
La capacidad reproductiva de estas arañas es relativamente baja, al menos bajo las condiciones del estudio, teniendo en cuenta que al parecer las hembras colocan un solo ovisaco durante su vida, con un número de huevos que oscila entre 23 y 128, y una viabilidad del 60.5%. No obstante, los muestreos en el campo permiten evidenciar densidades poblacionales altas con superposición de individuos en varios estadios de edades que van desde juveniles hasta adultos (Sabogal y Pinzón 2001).
Tanto la duración del ciclo de vida de
Se verificó que la ley de crecimiento constituye una herramienta efectiva para estimar el número de ínstares en estudios de ciclos de vida de arañas.
Footnotes
Agradecimientos
A COLCIENCIAS por su apoyo financiera (Proyecto: 1101-13-167-99); al Instituto de Ciencias Naturales de la Universidad Nacional de Colombia y a CORPOICA por el apoyo logístico; a la Dra. Nancy Barreto y al Dr. William Eberhard por su valiosa asesoría. A la Profesora Paulina Muñoz y a un evaluador anónimo por sus comentarios y sugerencias al manuscrito.
