Abstract
We began a fungi culture collection isolated from different Colombian regions, for uses in education, research and as potential biological agents. We collected 110 samples of vegetal material, dead insects and soil, from different vegetation communities, in the departments of Meta, Cauca, Cordoba and Cundinamarca. The fungal isolates were treated in culture media of defined composition. We identified 58 isolates with biocontrol potential. Of all the isolates, 3,2% were primary entomopathogenic, 20,6% phytopatogen controllers, 28,6% secondary entomopathogens and 47,6% possessed no biocontrol potential. Most of the fungi were isolated in the Department of Cauca (67% of the total number). 38,7 were derived from soil, 28,6% from plant material and 32,7% from insects, fruits and litterfall samples. The isolates were preserved in both soil and distilled water. Their macroscopic and microscopic morphological characteristics were evaluated 15, 45 and 90 days after collection. The preservation in distilled water was found to be the best method due to its low cost, ease of manipulation and recuperation of isolates. The isolates were evaluated in vitro against pesticides such as Furadan, Manzate, Malathion and Benlate at concentrations of 25 and 250 ppm. Manzate reduced the growth rate of all isolates significantly (p<0,01). With respect to the negative control, Furadan and Benlate inhibited the growth of all the isolates completely at both concentrations (p<0,01). This collection will serve as an important reference for future studies of these biological control agents (isolates) at molecular and physiological levels.
Introducción
Las numerosas especies de hongos biocontroladores, incluidas en los diferentes grupos taxonómicos, ofrecen amplias posibilidades de uso como agentes de regulación de poblaciones plaga y de enfermedades, presentándose nuevas perspectivas para la agricultura, debido a su facilidad de manejo, capacidad de esporulación y persistencia (Rodríguez 1990). La aplicación de microorganismos combinados con otros sistemas tradicionales de control, contribuyen a recuperar y mantener, de una manera más eficaz, el equilibrio entre las poblaciones de organismos presentes en los ecosistemas en general y en particular en los agroecosistemas (Astudillo 1993).
Algunos de estos hongos biocontroladores, los entomopatógenos, se registran en condiciones naturales bajo la forma de enzootias y pueden ocasionar epizootias importantes (Rodríguez 1984). Los hongos entomopatógenos más comunes son los Hyphomycetes, que atacan diferentes especies de importancia económica, especialmente del orden Lepidoptera y Coleoptera (Rodríguez 1990). La clase incluye géneros de hongos biocontroladores de enfermedades, como Trichoderma, Cladosporium, Penicillium y Fusarium no patógeno.
Por otra parte, los agroquímicos tienen una actividad tóxica sobre animales, plantas y ecosistemas en general, y se ha visto la necesidad de evaluar el efecto que sobre el crecimiento y esporulación de estos hongos, tienen algunos fungicidas, herbicidas, insecticidas y fertilizantes, que se usan corrientemente en la práctica agronómica. Sería importante utilizar de forma combinada alguno de estos productos con agentes de control biológico (Rodríguez 1990; Astudillo 1993; Atehortúa y Londoño, 1994; Rivera et al. 1994).
Los objetivos de este estudio consistieron en buscar hongos biocontroladores de microorganismos fitopatógenos y de insectos, en algunas regiones del país, con el fin de conformar un banco de cepas. Y caracterizar este banco de cepas con base en su compatibilidad con algunos plaguicidas químicos comerciales de uso común.
Materiales y Métodos
Recolección de muestras
Se colectaron muestras de suelo, insectos y material vegetal en diferentes grados de descomposición y no descompuesto, en varias localidades de los departamentos de Huila, Meta, Cundinamarca, Córdoba y Cauca. Las muestras se obtuvieron en diferentes ecosistemas naturales y agrícolas (Tabla 1). Éstas se depositaron en bolsas plásticas con cierre hermético o frascos plásticos tapa rosca estériles, de acuerdo con el tipo de muestra, las cuales se rotularon con la fecha, sitio de colección, clase de sustrato y comunidad vegetal. Las muestras se mantuvieron a 4°C hasta el momento de su procesamiento en el laboratorio.
Características de los lugares en las diferentes regiones colombianas donde se tomaron las muestras
Procesamiento de las muestras
Las muestras de material vegetal se procesaron por el método de dilución en placa (Wollum 1982). Se realizaron diluciones seriadas 1:10 hasta 10-3 en agua peptonada al 1% y se inoculó 0,1ml de las diluciones 10-2 y 10-3 en la superficie de los medio de cultivo: Agar Sabouraud Dextrosa (ASD), Agar Papa Dextrosa (APD) y Agar Extracto de Levadura-Glucosa- Cloramfenicol (YGC). Las muestras de insectos muertos, que presentaron crecimiento micelial externo, se sembraron directamente sobre el medio de cultivo, tomando una muestra de crecimiento del hongo sobre el insecto. Todos los medios de cultivo inoculados se incubaron a 25 ± 2°C por 5 días.
Identificación de los aislamientos
Al cabo de los 5 días de incubación, se aislaron para su identificación las colonias que crecieron en las cajas en APD o ASD. Ésta se realizó con base en la morfología macroscópica y microscópica de la colonia, usando las claves y descripciones de Domsch et al. (1980), Barnett y Hunter (1972), Gilman (1963), Nelson et al. (1983) y Thom y Raper (1945). En el caso de no observarse inicialmente estructuras reproductivas, las colonias aisladas se transfirieron a otros medios de cultivo como Agar Extracto de Malta (AEM) o Agar Agar (AA), y/ o se sometieron a diferentes condiciones de incubación: luz constante, choques de temperatura y otras, con el fin de inducir la producción de tales estructuras.
Conservación
Para la conservación de los aislamientos ya identificados se usaron tres métodos: 1) En tubos inclinados con ASD, los cuales, después de una incubación durante 7 días a 25 ± 2°C, se mantuvieron a 4°C. 2) En agua destilada estéril, en frascos de vidrio herméticamente cerrados. En 3 ml de agua destilada se suspendieron discos de aproximadamente 5 mm de diámetro cada uno de los aislamientos crecidos previamente en ASD o APD, durante 7 días a 25 ± 2°C. Posteriormente, se mantuvieron los frascos a 4°C, en oscuridad (Gilbert 1997, comunicación personal). 3) En suelo estéril. El suelo se esterilizó tres veces en autoclave a 110°C durante 1 ha 0,5 atm y se le realizó una prueba de esterilidad, sembrando varios granos de suelo sobre la superficie de ADS e incubando a 25 ± 2°C durante 7 días. Posteriormente, se depositaron 3 g de suelo en frascos de vidrio estériles a los cuales se inoculó 1 ml de una suspensión del aislamiento con una concentración de 1x106 conidios/ml. Los frascos se mantuvieron a 4°C.
La evaluación de estos métodos se hizo sembrando en la superficie de APD o ASD una porción de micelio del crecimiento en el tubo, una porción de suelo o uno de los discos de agar, de acuerdo con el método de conservación. Las cajas así inoculadas se incubaron a 25 ± 2°C por 7 días. Se evaluó cualitativamente la morfología macroscópica y microscópica de cada aislamiento.
Pruebas de compatibilidad con agroquímicos
Los aislamientos encontrados y registrados como potenciales biocontroladores se sometieron a una prueba de compatibilidad con 4 plaguicidas de uso común en la práctica agrícola. Para la prueba, la unidad experimental utilizada fue la caja de Petri y se empleó una modificación del método propuesto por Atehortúa y Londoño (1994). Los insecticidas carbofuran (Furadan) y malation (Malathion) y los fungicidas benomil (Benlate) y bis, ditiocarbamato de zinc (Manzate), se mezclaron, cada uno por separado, con el medio de cultivo (ADS), para una concentración final de 25 y 250 ppm.
Una vez preparadas las cajas, se inocularon con 0,1 ml de una concentración de 1 x 107 conidios/ml de cada aislamiento, provenientes del crecimiento de éste en ADS o APD a 25 ± 2°C por 10 días. La siembra de la suspensión conidial se realizó en un orificio de 1 cm de diámetro practicado en el centro del agar. Las cajas fueron luego incubadas a una temperatura de 25 ± 2°C por 10 días. Se realizaron tres réplicas por tratamiento y para cada aislamiento se utilizó un control negativo en el cual el medio de cultivo no contenía ningún plaguicida. Con el fin de determinar la compatibilidad se midió diariamente durante 10 días el diámetro de la colonia. Con estos datos se calculó la tasa de crecimiento diaria, en área, de cada aislamiento y el área de cubrimiento del crecimiento de cada aislamiento sobre la superficie del medio de cultivo, mediante la fórmula
Análisis estadístico
Los datos de las pruebas de compatibilidad se analizaron mediante análisis de varianza (Sokal y Rohlf 1981), con un nivel de significancia de 0,05, con el fin de establecer si había diferencia entre los tratamientos con los plaguicidas. Posteriormente, se utilizó la prueba de Mínima Diferencia Significativa (LSD), con un nivel de significancia de 0,05.
Resultados
Aislamientos fúngicos
Se procesaron 110 muestras de diferentes localidades de los departamentos de Huila, Cundinamarca, Cauca, Córdoba y Villavicencio. Se encontraron aislamientos de hongos con reconocido potencial entomopatógeno, controlador fitopatógeno y otros a los que no se les conoce ninguno de estos potenciales. Éstos están consignados en la colección de la Facultad de Ciencias de la Pontificia Universidad Javeriana. Los géneros identificados pertenecientes a cada uno de los grupos mencionados, las localidades y los sustratos a partir de los que se aislaron, se presentan en las tablas 2 y 3.
Hongos con potencial biocontrolador encontrados en los sitios de muestreo
Los insectos no se pudieron identificar por el alto grado de descomposición que presentaban.
Hongos sin potencial biocontrolador encontrados en los sitios de muestreo
Los insectos no se pudieron identificar por el alto grado de descomposición que presentaban.
El criterio utilizado para clasificar los hongos en las categorías entomopatógeno primario, entomopatógeno secundario, controlador de fitopatógenos y sin ninguno de estos potenciales, fue el conocimiento previo y los registros encontrados en la literatura, acerca de su comportamiento como patógenos, competidores, productores de sustancias antibióticas y tóxicas.
La mayoría de los aislamientos de los hongos se encontró en el departamento del Cauca (67% del total de las muestras procesadas), seguido por el departamento de Cundinamarca con el 59,5% y por el departamento del Huila con el 54% (Fig. 1).
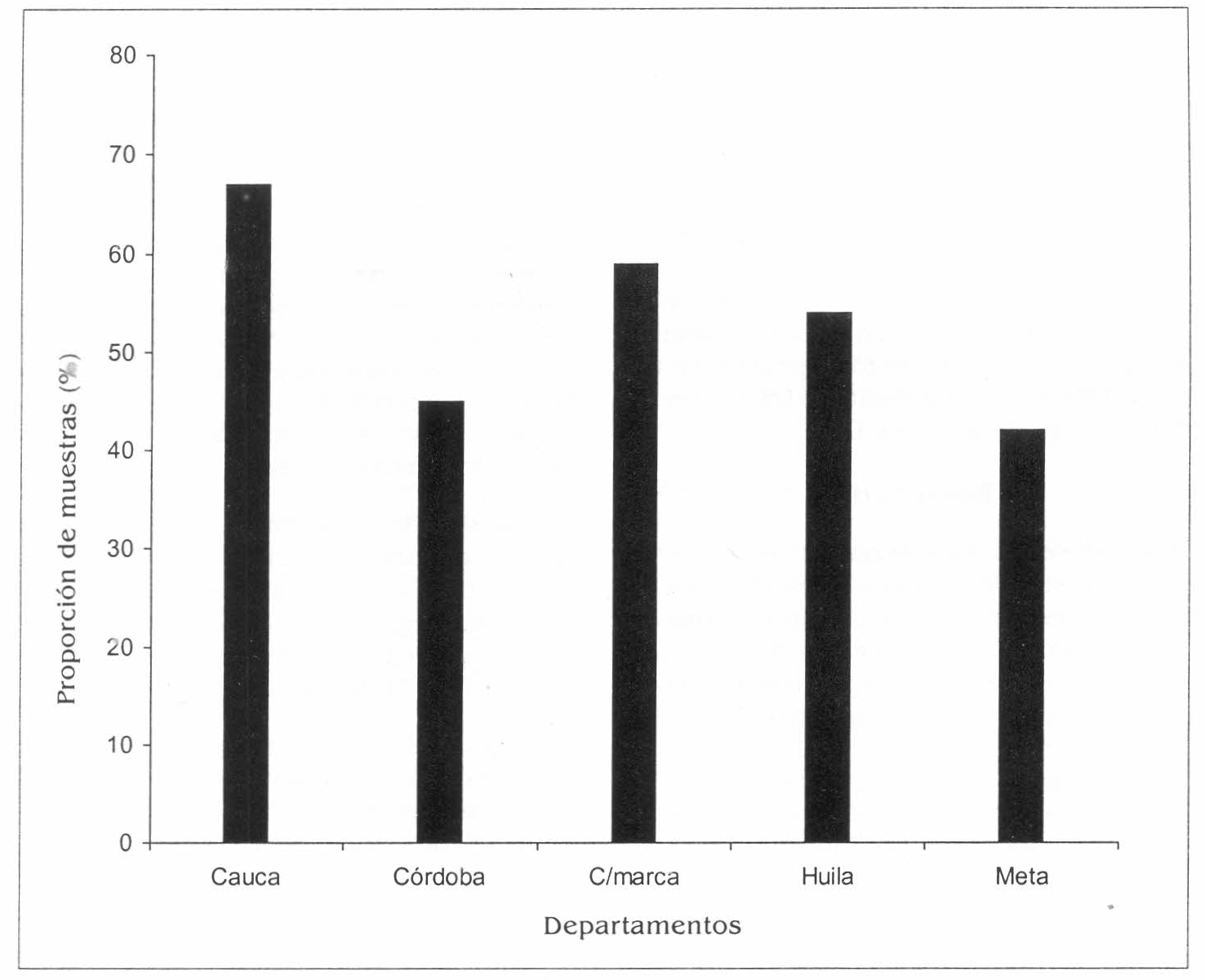
Proporciones de los aislamientos de hongos con potencial biocontrolados, en cada uno de los departamentos.
En cuanto al sustrato del cual se aislaron estas cepas, la mayoría (38,7%) de las muestras fueron de suelo y el resto, en porcentajes más bajos, estuvieron distribuidas entre los demás sustratos. El tipo de vegetación donde se aisló la mayor parte, fue bajo bosque natural, con el 28,6%. La recuperación de entomopatógenos fue muy baja (3,17% de las muestras procesadas), encontrándose en muestras de suelo y sobre insectos que estaban en las hojas de plantas que componen la vegetación natural. Solamente se halló Beauveria bassiana como hongo entomopatógeno primario. El 28,6% fueron hongos entomopatógenos registrados como secundarios, encontrándose aislamientos de Aspergillus sp., Fusarium oxysporum y Penicillium sp., que se consideran de esta manera, ya que se han aislado de insectos pero no se ha determinado claramente su actividad patógena frente a éstos. El 20,6% del total de las cepas aisladas (Fig. 2) correspondió a hongos registrados como biocontroladores, entre los cuales están Gliocladium sp., Fusarium sp. y Trichoderma sp., predominando este último género con más de 5 morfotipos y el 47,6%, hongos sin potencial biocontrolador registrado.
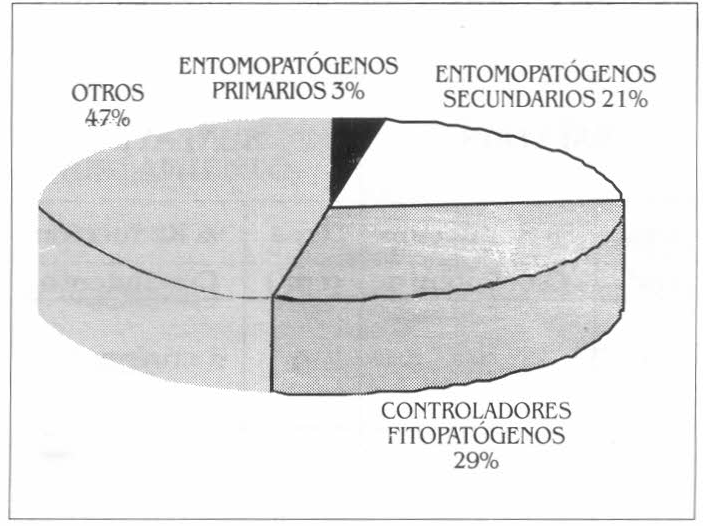
Distribución en porcentaje de cada uno de los grupos de hongos encontrados, de acuerdo con su capacidad controladora de fitopatógenos y de plagas de insectos o sin ninguna de estas actividades.
Dentro de los hongos entomopatógenos, tanto primarios como secundarios, se obtuvieron dos aislamientos de B. bassiana, los cuales se denominaron B. bassiana I y B. bassiana II. Estos aislamientos se recuperaron en el municipio de San Agustín (Huila) y en Montería (Córdoba), en ambientes con temperaturas medias de 19 y 28,3°C. Verticillium psallliotae se encontró sobre una araña (Eumetazoa: Chelicerata), en Cundinamarca, con cobertura vegetal de bosque altoandino húmedo (Reserva Natural de Chicaque). Se halló Penicillium spp. en suelo. En el Chepero (Meta), Mata de Plátano (Córdoba) y Mesitas (Huila), se identificaron especies del género Aspergillus hasta el nivel de grupo: clavatus, flavusoryzae y niger. Fusarium oxysporum se aisló de suelo de cultivo de maíz, sobre hojas secas de arveja en el municipio de San Agustín (Huila) y sobre un insecto adulto, muerto, no identificado hallado en suelo con vegetación de bosque altoandino húmedo en Cundinamarca. Fusarium moniliforme se aisló de un insecto muerto encontrado en bosque altoandino húmedo.
Con relación a los hongos controladores de fitopatógenos, se obtuvieron varios aislamientos de Trichoderma sp. tanto bajo vegetación nativa como de cultivos, Mortierella sp. en suelo, también bajo distintos tipos de vegetación en Córdoba y Meta. Gliocladium roseum, aislado de suelo superficial en cultivo de palma de Cumare en Cumaral (Meta).
Dentro de los aislamientos identificados sin potencial biocontrolador se encontró Geotrichum sp., Fusarium reticulatum, Fusarium decemcelullare, Fusarium proliferatum, Fusarium equiseti, Aspergillus del grupo fumigatus, Micogone sp., Scopulariopsis sp., Acremonium fusidiodes, Botrytis sp. y Cylindrocladium parvum. Todos éstos pertenecen al Phylum Ascomycota, Clase Ascomycetes, grupo Deuteromycetes, de acuerdo con Alexopoulos et al. (1996).
Conservación de los aislamientos
La recuperación de los aislamientos, después de su conservación con el método de agua destilada y de suelo, arrojó como resultado que todos mantuvieron las características morfológicas tanto macroscópicas como microscópicas originales. Esto se presentó en todos los períodos de tiempo evaluados. Para el caso de la conservación en medio de cultivo, fue necesario realizar pases periódicos cada 30 - 40 días, con el fin de mantener la viabilidad de los aislamientos.
Compatibilidad con plaguicidas
Tanto el área de crecimiento de cada uno de los aislamientos después de 10 días frente a 25 ppm de los agroquímicos evaluados, como el porcentaje de reducción de su crecimiento con respecto al control negativo, se muestra en la Tabla 4. El rango de inhibición que presentaron los aislamientos frente al carbofuran estuvo entre el 11 y 30%, para el bis, ditiocarbamato de zinc entre el 0 y 87%, para el malation entre el 0 y 35% y para benomil entre el 21 y 100%. El compuesto que más afectó a los hongos aislados fue benomil, seguido por el bis, ditiocarbamato de zinc, el cual generó, además de un rango amplio de inhibición, una alta variabilidad en la tasa de crecimiento diametral de los aislamientos.
Área y porcentaje de reducción de la tasa de crecimiento en área de cada uno de los aislamientos identificados con potencial biocontrolador, evaluados frente a 25 ppm de cada uno de los 4 plaguicidas
El área y el % de reducción del crecimiento corresponden al promedio de tres repeticiones.
Frente a una concentración de 25 ppm de que con 250 ppm de los fungicidas y de los insecticidas, los aislamientos mostraron una menor inhibición en la tasa de crecimiento (Tablas 4 y 5). Con el bis, ditiocarbamato de zinc se presentó una gran variabilidad en el efecto de reducción de dicha tasa (Tabla 4). Por su parte, malation, a las dos concentraciones, redujo la tasa de crecimiento solamente del aislamiento B. bassiana I de manera muy significativa respecto al control (p=0,001 en ambas concentraciones). El bis, ditiocarbamato de zinc a 25 y 250 ppm redujo diferencialmente la tasa de crecimiento de las cepas, pero produciendo una reducción muy significativa sólo para A. flavus, A. clavatus, F. moniliforme y Mortierella sp. (p=0,001). La mayoría de los hongos alcanzaron el 100% de crecimiento (respecto al control negativo), a los 10 días, con las dos concentraciones empleadas de todos los plaguicidas, con excepción del benomil. En términos generales, los hongos presentaron una mayor inhibición con los insecticidas (en ambas concentraciones) que con los fungicidas.
Área y porcentaje de reducción de la tasa de crecimiento en área de cada uno de los aislamientos identificados con potencial biocontrolador, evaluados frente a 250 ppm de cada uno de los 4 plaguicidas
El área y el % de reducción del crecimiento corresponden al promedio de tres repeticiones.
Al comparar el área final de cubrimiento del crecimiento sobre el agar, de cada uno de los aislamientos enfrentados tanto a 25 como a 250 ppm de los plaguicidas, se encontraron diferencias altamente significativas entre los aislamientos (p= 0,0001). Con respecto a los plaguicidas, benomil inhibió muy significativamente el área de crecimiento de todos los aislamientos (p<0,01), con respecto al control, en ambas concentraciones. El malation y el bis, ditiocarbamato de zinc a 25 y 250 ppm, redujeron ligeramente el área de crecimiento de todos los aislamientos con respecto al control negativo, pero de manera fue muy significativa (p=0,001); F. oxysporum fue la excepción con el malation. En contraposición, el carbofuran no redujo el área de cubrimiento de ningún aislamiento respecto al control (p=0,72).
Discusión
Aislamientos fúngicos
Las comunidades vegetales donde se encontró una mayor proporción de hongos entomopatógenos y de hongos controladores de fitopatógenos fue bajo vegetación natural (bosque altoandino húmedo y páramo) con 54%. El hecho de encontrar una mayor proporción de hongos en bosque natural puede explicarse debido a que la vegetación en estos bosques ayuda a regular la humedad y temperatura, evitando de esta manera fluctuaciones bruscas de estos parámetros, crea hábitats variados por su complejidad estructural; además, no está sometida a la aplicación de agroquímicos. Todo esto hace que sea un ecosistema con condiciones apropiadas para el mantenimiento de la microbiota natural. La mayor recuperación de aislamientos fue bajo vegetación natural, pero bajo vegetación de diferentes cultivos hubo una recuperación relativamente alta (46%), lo que indicaría que a pesar del manejo cultural con frecuentes aplicaciones de fungicidas y otros productos químicos, que pueden afectar la supervivencia y el crecimiento de los hongos, hay todavía condiciones favorables que permiten su persistencia en estos ambientes, como por ejemplo restos vegetales e insectos.
En este mismo marco, aunque el número de muestras obtenidas en los departamentos de Córdoba, Meta y Cauca fue similar (entre 11 y 15), en las muestras de este último departamento fue donde se obtuvo una mayor cantidad de aislamientos con potencial biocontrolador (67%), respecto a 53% de Córdoba y 45% del Meta. Esto pudo deberse en parte, a que la mayoría de las muestras del Cauca provinieron de sustratos bajo vegetación natural y por el contrario, en Córdoba y Meta, éstas fueron de vegetación de cultivos.
Por otra parte, la mayor proporción de aislamientos se obtuvieron a partir de las muestras de suelo, lo cual no sólo podría reflejar que es un hábitat favorable para los hongos, sino que la mayor parte de las muestras colectadas eran de este sustrato y además hubo una buena recuperación de aislamientos. El caso de los insectos fue totalmente inverso, en el sentido que el número de muestras de este tipo fueron pocas y además la recuperación de aislamientos no fue fácil.
En general, la recuperación de hongos con potencial biocontrolador fue relativamente baja con respecto al total de hongos. Esto puede ser el resultado de la interacción de por lo menos tres factores: 1) el reflejo de la proporción de hongos con este potencial en los sustratos colectados bajo las condiciones prevalentes, 2) la utilización de medios de cultivo sintéticos que no favorecen su recuperación desde el punto de vista nutricional, y 3) el método empleado de diluciones seriadas. Con referencia particular a los cultivos de maíz, no se encontró ningún hongo entomopatógeno, en comparación con estudios de otros autores como Rodríguez (1984), quien registró especies como Nomurae rileyi en este tipo de cultivo.
Entre los hongos entomopatógenos encontrados, B. bassiana ha sido uno de los más estudiados (Campbell et al. 1985; Rombach et al. 1986; Anderson et al. 1988; Ming-Guan y Jonson 1990; Leathers y Gupta 1993; Varela y Morales 1996). Es conocido agente causal de muscardinas en gusanos de seda; en las regiones cafeteras de Colombia es utilizado en el control biológico de broca del café, así como también contra especies de defoliadores como Sibinefusca sp., Euprosterna eleasa, Osiphanes cassina y Oiketicus sp. en cultivos de palma de aceite; también contra Collaria columbiensis (chinche de pastos) (Benavides, sf.; Rodríguez y Benavides 1994; Calvache 1995). Trabajos realizados en CENICAFÉ, en los cuales se han hecho aspersiones de este hongo en los cafetales, muestran la inducción de epizootias (Vélez 1996). También se ha registrado como agente de control biológico en otras especies de diferentes órdenes, que son plaga en diversos cultivos de importancia económica, entre las cuales se puede mencionar: Manalion dissimulatum Distant (Hemiptera: Miridae), Blissus insularis Barber (Hemiptera: Lygaeidae), Acanthoscelides obtectus Say (Coleoptera: Bruchidae), Cosmopolites sordidus Germar (Coleptera: Curculionidae), Anticarsia gemmatalis (Hubner) (Lepidoptera: Noctuidae), Sitophylus oryzae Linnaeus (Coleoptera: Curculionidae) y Diatrea saccharalis Fabricius (Lepidoptera: Pyralidae) (Vélez 1985). En este estudio se encontró B. bassiana en bosque natural, lo cual indica que es un habitante normal de bosques, donde puede estar contribuyendo a la regulación de poblaciones de insectos.
Los dos aislamientos de B. bassiana, I y II, se encontraron en ambientes con temperaturas distintas (19 y 28°C). Esto concuerda con lo registrado por Domsch et al. (1980), quien menciona que este género está en regiones tropicales a temperaturas muy variadas, aunque muestra mejor crecimiento en ambientes con clima cálido a templado. La especie hallada es la más extensamente distribuida del género y generalmente está formando ramilletes de conidios pulverulentos y blancos sobre diferentes clases de insectos de los órdenes Lepidoptera, Coleoptera e Hymenoptera (Domsch et al. 1980; Rodríguez 1984).
V. psalliotae mostró la capacidad que tiene para crecer en ambientes con una temperatura óptima de 23 - 24°C y mínima de 8 - 10°C, confirmando los registros de Domsch et al. (1980), quienes mencionan el hallazgo de esta especie en suelos de bosques naturales en Estados Unidos. Esta especie se ha registrado como controlador de royas y se ha aislado de ácaros del suelo, de chicharras y de insectos del orden Lepidoptera, Sin embargo, por el sustrato de donde se aisló en este estudio, podría estarse comportando como un patógeno secundario, dado que no hay literatura referente a su ataque sobre artrópodos, para producirles la muerte y el solo hecho de hallarlo en la araña no permite confirmar su carácter patógeno sobre artrópodos. Se sabe que las arañas son benéficas en la mayoría de los casos, por lo que se requeriría realizar bioensayos de patogenicidad con este aislamiento, con el fin de confirmar su carácter patógeno sobre este artrópodo. Esto serviría como base para la utilización de esta especie como agente de control biológico, en casos de tener explosiones de poblaciones de arañas en cultivos. La araña sobre la que se encontró no pudo ser identificada dado su estado avanzado de descomposición. Esta especie de hongo ha sido registrada como micoparásito de Rhopalomyces elegans (Domsch el al. 1980), por lo que puede ser promisoria para el control de hongos fitopatógenos (Saksitirat y Hoppe 1991).
En Colombia, el género Penicillium se ha registrado en la región panelera del Río Negro (Cundinamarca), en larvas de Dietreee saccharalis Fabricius, del cual se consideró como patógeno secundario (López el al. 1983). En la localidad de Villeta (Cundinamarca) se registró atacando especies de Lepidoptera: Pyralidae en caña panelera (Rodríguez 1984). Este género ha sido considerado en la literatura como biocontrolador pues posee, además de su capacidad parasitaria, la capacidad de producir compuestos o metabolitos de carácter tóxico (antibióticos, nematicidas y fungistáticos). Sin embargo, en este estudio se consideró al género Penictltium como un saprófito y no como entomopatógeno, dado que se aisló de las muestras de suelo tanto bajo vegetación nativa como de cultivos agrícolas en localidades del Huila, Cauca, Cundinamarca, Meta y Córdoba, pero nunca de insectos. Dada la amplia distribución de este género, se comprueba así su gran capacidad de adaptación a diversos climas y condiciones. En el departamento del Cauca se encontró al nivel de páramo, lo que indica que este género puede persistir a temperaturas bajas (6 - 10°C), aunque su temperatura óptima de crecimiento es de 25°C. Las especies del género predominan en suelos de regiones templadas y tropicales, han sido detectadas a grandes profundidades y están en pequeñas concentraciones en la rizosfera (Domsch el al. 1980). Muchas especies de Penictllium han sido estudiadas al nivel de control biológico. Entre ellas está P. breuicompeciurn, la cual presentó antagonismo tanto in vitro como in vivo frente a Botrutis fabae en cultivo de habas, por producir antibióticos (Jackson el al. 1997).
El género Aspergillus del grupo clavalus ha sido aislado de insectos, particularmente de abejas adultas muertas y de panales; también en plumas y excrementos de pájaros de vida libre. Se ha encontrado en almacenamiento de varios productos alimenticios, incluyendo semillas de sorgo, arroz, productos de harina y pastas (Domsch et al. 1980). Se presenta más como parásito que como entomopatógeno; además en este estudio se halló en suelo con un alto contenido de humedad, en la vereda Chepero, municipio de Cumaral (Meta), mostrando así su capacidad de crecer y permanecer en regiones tropicales y subtropicales (Domsch el al. 1980). Las especies de Aspergillus, del grupo flavus tienen una distribución amplia en regiones tropicales y subtropicales; no se han registrado como entomopatógenos, pero sí se han aislado en diferentes insectos del orden Lepidoptera, en Cundinamarca (Rodríguez 1984). Este hongo produce aflatoxinas, que comúnmente se encuentran en productos alimenticios y que, al ser ingeridas, producen intoxicaciones graves en animales y en el hombre (Samson el al. 1984; Scott 1989) y enfermedades cancerígenas a nivel hepático (Giral el al. 1989). Por esta razón, se necesitaría evaluar minuciosamente este hongo antes de ser utilizado en programas de control biológico. Sin embargo, se han registrado estudios de formulaciones con alginato de cepas atoxigénicas de A. flavus (Daigle y Cotty 1995), como una buena alternativa para su uso al nivel de campo, puesto que el alginato estimula la esporulación e impide el antagonismo. Haría falta evaluar la formulación y las cepas bajo condiciones que favorezcan epidemias de contaminación por aflatoxinas en diferentes suelos, con el fin de evaluar su eficacia. En este estudio, se encontró en suelo con cultivos de maíz y yuca en Montería, confirmando así su presencia en localidades de temperaturas cálidas. Las del grupo niger presentan una distribución mundial restringida a la región tropical; tienen gran capacidad de producción de metabolitos tóxicos y poseen un efecto inhibitorio ante especies como Fusarium oxysporum, Trichoderma polysporum y Penicillium niqricens, entre otros. En este estudio se aisló de diferentes muestras y en localidades de los departamentos de Huila, Cauca y Cundinamarca, lo que confirma que tienen una amplia distribución en distintos ambientes. Sería importante comprobar su actividad controladora y tóxica para emplearse en control biológico.
F. oxysporum se encontró sobre sustratos en los que se puede estar comportando como saprófito y sobre un insecto que no pudo ser identificado. Ya que se ha registrado esta especie como patógeno de insectos del orden Lepidoptera y a pesar de ser fitopatógeno se ha encontrado parasitando huevos, hembras y quistes de H. glicines (Cotes 1997; Rodríguez 1984), es posible que su papel en el insecto hubiese sido como entomopatógeno primario. Adicionalmente tiene buenas perspectivas para usarse como controlador biológico, ya que ha mostrado que puede causar la muerte de algunos insectos plaga como Diatrea saccharalis (Fabricius) y Antigastra catalanalis (Duponchel) (Rodríguez 1984). En el reconocimiento de enemigos naturales de la broca del café, Hypothenemus hampei (Ferrari), realizado por la Disciplina de Entomología de CENICAFÉ, se ha observado la presencia de F. oxysporum y F. solani sobre la broca, en diferentes localidades de la zona cafetera (Pérez et al. 1996). Sin embargo, en este último caso, no ha establecido su carácter entomopatógeno primario. Su uso como controlador biológico debe evaluarse cuidadosamente debido a que es fitopatógeno de varias plantas de cultivo.
Fusarium moniliforme se aisló a partir de un insecto muerto no identificado, en el cual puede estar actuando como saprófito, ya que no se ha registrado como entomopatógeno. Habría que establecer esta capacidad con pruebas de patogenicidad y en caso dado, definir su implementación en programas de control biológico dada su patogenicidad para plantas de maíz y su toxicidad para patos, embriones de pollo, gallo y algunos mamíferos (Domsch et al. 1980).
Trichoderma sp. es uno de los hongos más utilizados como agente de control biológico de fitopatógenos, a través de la producción de sustancias tóxicas, de la competencia por nutrientes, espacio u oxígeno, o del parasitismo. Se han registrado resultados positivos en el control de enfermedades en pimiento, tomate y tabaco en Cuba (López y Rijo 1994). En Colombia se han realizado varios ensayos demostrando su capacidad antagónica contra F. oxysporum, que ocasiona marchitamiento vascular del clavel, entre otros cultivos (Ochoa 1996).
Gilman (1963) registró aislamientos de Mortierella sp. de suelos de diferentes partes del mundo, considerándolo como un buen biocontrolador de fitopatógenos. Para su utilización práctica en este sentido, habría que explorar más sus propiedades y capacidades biocontroladoras de fitopatógenos, ya que poco se sabe de este género en ese sentido. Gliocladium roseum se ha presentado como biocontrolador, específicamente como parásito de hongos fitopatógenos como Botrytis sp., Ceratocystis sp. y Trichotecium sp., por lo cual tiene gran importancia para aplicaciones en control biológico (Cotes 1997).
Métodos de conservación
El método de conservación en agua destilada se ha empleado para la preservación de hongos, ofreciendo muy buenas perspectivas para su uso, ya que es un método muy económico, fácil de mantener, práctico para el almacenamiento y la recuperación, y favorable para el mantenimiento de aislamientos fúngicos. Se ha registrado que este método es adecuado para el mantenimiento de aislamientos de hongos provenientes de material vegetal y del suelo, hasta por 7 años (Gilbert 1997, comunicación personal). Es necesario evaluar el método para hongos con potencial biocontrolador por un período más prolongado de tiempo, con el fin de determinar su eficacia para este tipo de aislamientos. El método de conservación en suelo también es bastante económico, aunque un poco más dispendioso que el anterior. Esto último se debe a la esterilización previa que debe hacerse del suelo con el fin de eliminar por completo la microbiota nativa de éste y a las pruebas de esterilidad que deben practicarse antes de la inoculación del aislamiento fúngico.
Compatibilidad con plaguicidas
La compatibilidad que presentan algunos productos agroquímicos con hongos que poseen potencial biocontrolador, es de gran ayuda para la incorporación del control biológico con hongos, dentro de programas de manejo integrado de plagas (MIP). Los plaguicidas evaluados Carbofuran, Malation, Bis, ditiocarbamato de zinc y Benomil, son usados en el campo en diferentes dosificaciones, dependiendo de varios factores, entre los que se incluyen: el tiempo a partir de la siembra, el grado de infestación por la plaga y el cultivo que se desea asperjar. Estos productos son utilizados en cultivos de papa, arroz, plátano, banano y algodón, entre otros. Aunque las concentraciones evaluadas son, en términos generales, entre 10 y 4000 veces menores que las usadas en campo, éstas fueron escogidas con base en estudios previos (Astudillo 1993; Atehortúa y Londoño 1994; Rivera et al. 1994; Rivera 1993), en los cuales concentraciones más altas de Benomil y Malation inhiben completamente la esporulación en algunos géneros fúngicos usados también en este estudio. La concentración más baja utilizada (25 ppm) es 10 veces menor que la más alta (250 ppm), pero el porcentaje de inhibición del crecimiento no fue proporcionalmente mayor, lo cual señala que no hay una relación lineal entre la concentración de estos plaguicidas y el efecto de reducción o inhibición que causan sobre el crecimiento de los aislamientos fúngicos.
Los insecticidas usados atacan principalmente las células nerviosas de los insectos, pero como se demostró en este estudio, pueden presentar actividad negativa contra los hongos, reduciendo su tasa de crecimiento. Adicionalmente, dada la respuesta diferencial de aislamientos de la misma especie (B. bassiana, en este caso particular), frente a estos insecticidas, en particular al Malation, se propone su uso como herramienta dentro de la caracterización de aislamientos fúngicos con miras a su utilización en control biológico. Habría que probarlo con otras especies para establecer con seguridad esta posibilidad.
El Benomil y el bis, ditiocarbamato de zinc tienen efectos fungicidas comprobados, pero no todos los hongos responden de la misma manera, como se vio en este estudio. El Benomil es un fungicida más efectivo, dado que inhibió completamente el crecimiento de todos los aislamientos o lo redujo de manera muy significativa. El bis, ditiocarbamato de zinc, por su parte, redujo la tasa de crecimiento de algunos: A. flavus, A. clavatus, F. moniliforme y Mortierella sp., pero sólo con respecto al control negativo.
En general, carbofuran, malation y bis, ditiocarbamato de zinc ejercieron solamente un efecto inhibitorio sobre los aislamientos usados, mientras que benomil sí tuvo un efecto biocida sobre grupos de hongos taxonómica y fisiológicamente diferentes. La evaluación realizada en este estudio fue al nivel del crecimiento de los hongos (tasa de crecimiento y área final de cubrimiento), pero puede hacerse a otros niveles como de esporulación, de germinación, genético o de producción enzimática, lo que daría una indicación de los niveles al que están actuando los productos.
Conclusiones
En general, los hongos identificados en este estudio se determinaron como entomopatógenos primarios o secundarios, y como controladores de fitopatógenos, con base en los registros existentes en la literatura sobre el género o la especie en particular. Así, es necesario comprobar su capacidad patogénica haciendo bioensayos, utilizando incluso diferentes aislamientos de un mismo género. Independientemente de la controversia acerca de si usar aislamientos de una región para ser aplicados en la misma o más bien usar los de otra región, se sugiere probar inicialmente con aislamientos de la misma región o cultivo, dado que estarían más adaptados a las condiciones medio ambientales prevalentes.
De acuerdo con los resultados encontrados en este estudio, se sugiere el empleo de malation, carbofuran y bis, ditiocarbamato de zinc conjuntamente con hongos agentes de control biológico, con diferencias temporales de aplicación y/o en dosis más bajas, con el fin de reducir el impacto sobre los hongos. Necesariamente habría que realizar evaluaciones previas para determinar estos tiempos y concentraciones.
La colección intensiva de hongos con potencial biocontrolador es esencial para rescatar y mantener ex situ el germoplasma de éstos, sobre todo el proveniente de ecosistemas naturales, donde existe una regulación natural de las poblaciones plaga. De esta manera se tendrá la fuente para la implementación en agroecosistemas. Tal colección es el punto inicial para una futura selección y establecimiento de su potencial biocontrolador con miras a implementarlos en control biológico. Además hay que considerar la posibilidad de que sirvan como fuente de metabolitos que pueden ser usados con estos y otros fines.
