Abstract
Introduction of a species of psyllidae attacking young tissues of different Eucalyptus species, is known from Australia, where it is native, Europe, North and South America since the 1800's. The Psillidae began to be found in second turn plantations of E. globulus Labill surrounding the Sabana of Bogota in 1994. In order to confirm its taxonomical identity as well as to investigate its biology, habits, natural enemies and damage characteristics, observations in field, greenhouse and semicontroled conditions in laboratory (15°C y 80% H.R.) were performed. This species of psyllidae was identified as Ctenarytaina eucalypti Maskell and is believed to be a potential pest in Colombian forests. The occurrence of two to three generations per year was determined, as well as the morphological characteristics, biology and habits of each one of the development stages that occur in young branches and leaves in nursery and second growth plantations. Natural control of this species of Psyllidae is achieved by predators of two species of Syrphidae (Diptera) and one of Hemerobiidae (Neuroptera). A preliminary laboratory test suggests that the Syrphidae species is a more efficient predator of the studied species of Psyllidae than is the hemorobiid.
Introducción
Ctenarytaina eucalypti Maskell es conocido como el psílido del eucalipto. Esta especie, como su hospedero, es originaria de Australia y fue introducida accidentalmente en Nueva Zelanda a fines de 1800, luego llegó a Inglaterra y posteriormente pasó a Portugal, España e italia (Cibrian et al. 1995; Cadahia 1980; Cavalcaselle 1982). Según Cadahia (1980), este pulgón llegó a España en 1972, ocasionando problemas en plantaciones jóvenes y en viveros de varias especies de eucalipto, con predominio en E. globulus. La presencia de este insecto ha sido registrada en el continente africano en Burundí, Tanzania, Etiopía (Azevedo y Figo 1979), en la región de Tanneron en Francia durante 1994 y 1995 (Bertaux et al. 1996), California (Dreisdat et al. 1994). С. eucalypti se registró por primera vez para Sur América en Uruguay, como plaga en varias especies de eucalipto, entre las que se encuentra E. globulus (Morey et al. 1995). En Bolivia se han observado altas infestaciones en el E. globulus, que generan inquietudes en los productores pero que en realidad no ocasionan perjuicios a las plantaciones (Boa y Bentley 1997). En Colombia, la posible presencia de C. eucalypti, fue registrada en rebrotes de plantaciones de E. globulus, y posteriormente confirmada y señalada por primera vez para Colombia (Pinzón 1997; Pinzón et al. 1999).
En California, C. eucalypti presenta de tres a cuatro generaciones por año dependiendo de las condiciones climáticas y la disponibilidad de plantas (Dahlsten et al. 1996). La duración del desarrollo total de una generación o ciclo de vida del insecto a 18°C y 70% de humedad relativa puede considerarse de un mes aproximadamente y en grandes infestaciones se superponen estados y generaciones (Azevedo y Figo 1979; Cadahia 1980; Cibrian et al. 1995). Los daños ocasionados por este pulgón son registrados en varias especies de eucalipto y al respecto se tienen diferentes opiniones sobre las consecuencias de sus infestaciones que varían desde registros que lo catalogan como insecto perjudicial, hasta aquellos que no consideran sus infestaciones como de importancia económica dado que no causan muerte de árboles. El daño causado por los psyllidae es principalmente estético y por lo tanto la tolerancia varía entre las personas, las plantas afectadas y la localización de los cultivos (Dalshten et al. 1996; Azevedo y Figo 1979). Cuando el follaje del eucalipto es usado con fines ornamentales por la industria floral, la infestación con el pulgón ocasiona efectos estéticos indeseables que son contrarrestados con control químico como ocurre con E. pulverulenta en California (Dalhstein et al. 1996)
Se considera que el daño de C. eucalypti puede ser significativo en relación con la disminución del desarrollo, como consecuencia del ataque en hojas primordiales. Cuando los crecimientos son lentos y se prolonga la permanencia de las poblaciones en el follaje juvenil, los brotes tiernos llegan a secarse produciendo bifurcación de guías terminales y deformaciones que retrasan el desarrollo de los árboles (Cadahia 1980). Según Pirone, citado por Porcile 1998, cuando esto ocurre los daños son perjudiciales y los brotes se ven afectados, por lo que recomienda la aplicación de carbaryl o piretroides. Ciesla et al. (1996) mencionan a C. eucalypti como la plaga forestal más importante de Portugal, siendo causante de distorsión y marchitamiento de puntas de ramas, muerte de ramas y reducción del crecimiento en plantas jóvenes debido a la pérdida de follaje. Las ninfas y adultos secretan mielecilla ocasionando desarrollo de fumagina sobre el tejido.
Los psyllidae son controlados en forma natural por avispas parásitas de la familia Ichneumonidae y depredadores como larvas de moscas de las familias Syrphidae y Sciaridae, coleópteros de la familia Coccinelidae, odonatas, arácnidos y pájaros (Azevedo y Figo 1979; Philips, citado por Porcile 1998; Porcile 1998; Cadahia 1986; Cadahia y Ruperez 1979; Bertaux et al. 1996). Chauzat y Purvis (2000) señalan un parasitismo de 100% de las poblaciones de psyllidos en plantaciones comerciales en Kerry (Irlanda) mediante control biológico clásico con el parasitoide Psyllaephagus pilosus Noyes (Hym.: Encyrtidae), introducido desde Australia, inicialmente a Francia y de allí a Irlanda.
El presente trabajo tuvo como objetivos confirmar la identificación taxonómica del pulgón encontrado en viveros y plantaciones de segundo crecimiento de E. globulus, en la sabana de Bogotá, caracterizar la morfología y hábitos de cada estado de desarrollo, ciclo biológico, características de daño y reconocimiento de enemigos naturales presentes en el área de estudio. Para ello se contó con apoyo económico por parte del Centro de Investigaciones y Desarrollo Científico de la Universidad Distrital Francisco José de Caldas.
Materiales y Métodos
Aspectos taxonómicos
Para llevar a cabo la confirmación taxonómica de la especie plaga y sus enemigos naturales, se colectaron estados inmaduros y adultos en rebrotes y árboles de regeneración natural de E. globulus visiblemente infestados. Las muestras preservadas en alcohol al 70% se enviaron al Museo de Historia Natural con sede en Londres.
Biología, hábitos y enemigos naturales
Las observaciones sobre la biología del pulgón, así como de sus enemigos naturales se realizaron en el laboratorio de Sanidad Forestal de la Facultad del Medio Ambiente y Recursos Naturales de la Universidad Distrital, a temperatura promedio de 15°C y Humedad Relativa promedio de 80%, registradas diariamente en un higrotermógrafo Haenni.
Las observaciones sobre hábitos y duración de cada uno de los estados de desarrollo del insecto plaga se llevó a cabo seleccionando individuos recién emergidos, tomados de puntas de ramas de E. globulus infestadas naturalmente en campo. Se hicieron observaciones diarias para establecer con certeza el momento de cada muda. Cada vez que ocurrió una muda el individuo fue transferido a una nueva rama, con el objetivo de evaluar la duración de este nuevo ínstar hasta completar 100 observaciones para cada estado de desarrollo. Con las hembras y machos adultos obtenidos y mediante aislamiento por parejas se realizaron algunas observaciones de comportamiento reproductivo.
Caracterización del daño
La metodología utilizada para evaluar el daño fue adaptada a partir de aquella desarrollada para medir el grado de esclerofilia en hojas de eucalipto (Steinbauer et al. 1998), mediante la comparación de peso seco/cmβ de área foliar en ramas infestadas versus ramas no infestadas, de un grupo de cincuenta plántulas provenientes de un vivero comercial de tres meses de edad, a los cuales se realizó poda total de ramas laterales para homogeneizar la edad de los rebrotes. Una vez éstos alcanzaron un mínimo de 10 cm de longitud, se realizó la infestación, mediante la aproximación de puntas de ramas infestadas provenientes de campo. En cada árbol se mantuvo una rama infestada con jaula para medir el efecto de la alimentación del insecto, una rama no infestada con jaula para medir el efecto de esta última y una rama testigo sin infestación y sin jaula. Una vez se observó atentamente la colonización, al cabo de 56 días se empezaron a realizar las evaluaciones a grupos de tres árboles por semana; para ello se cortó cada rama hasta el tercer par de foliolos, contando el número de individuos presentes y estableciendo el peso seco/cmβ. De esta manera, esta comparación se desarrolló como un diseño completamente al azar en donde los tratamientos correspondieron al tipo de rama (infestada, jaula, testigo) y número de días de exposición a la infestación, siendo el rango de este último de 56 a 125 días, obteniendo como resultado final 33 tratamientos con 3 repeticiones cada uno.
Enemigos naturales
El reconocimiento de agentes de control natural se llevó a cabo mediante búsquedas y observaciones en árboles de rebrote y de regeneración natural. Se hicieron capturas de estados inmaduros de dípteros y neurópteros, los cuales se llevaron al laboratorio para evidenciar el grado de asociación con la especie plaga. Estas observaciones permitieron la diferenciación y caracterización de cada una de las especies, grado de asociación, caracterización biológica preliminar.
Con posturas obtenidas a partir de individuos adultos, se realizaron algunas observaciones preliminares sobre capacidad de depredación, ofreciendo cada 24 horas 20 presas en los estados ninfales 1 y 2 para el ínstar 1, 20 en estado 3 y 4 para el ínstar 2 y 30 en estado 5 y adulto para el ínstar 3, cuya comparación se llevó a cabo mediante un análisis de variación de una vía, con tres tratamientos correspondientes a los tres predadores analizados, cada uno de los cuales contó como mínimo con 30 repeticiones.
Resultados y Discusión
Aspectos taxonómicos
El pulgón del E. globulus fue determinado como Ctenarytaina eucalypti (Maskell, 1890) (Hemiptera: Psylloidea: Psyllidae (D. Hollis (NHM) det.). De esta forma se confirmó en Colombia la presencia de esta especie cuya distribución paulatina en diferentes países del continente americano se viene registrando durante la última década. A pesar de que la especie es oligófaga en nuestro país ha sido observada hasta el momento únicamente en E. globulus.
Características morfológicas, biología y hábitos
El pulgón del eucalipto es un insecto de metamorfosis gradual que pasa por los estados de huevo, cinco ínstares ninfales y adulto. En la tabla 1 se resume la duración de cada uno de los estados de desarrollo del insecto y en las figuras 1-3 se muestran características de las infestaciones y de los diferentes estados de desarrollo, respectivamente.
El huevo presenta un tamaño promedio de 0.13 mm de ancho y 0.34 mm de largo. Los huevos son puestos por las hembras adultas en las axilas de las hojas apicales, aunque también se observan en la lámina foliar y en las ramitas. Se les puede ver formando grupos de número variable, conformados por huevos en diferentes estados de maduración. Son de forma oval y permanecen adheridos a las hojas por el pedicelo (Fig. 1). El corion es de color blanquecino; aunque dependiendo del estado de desarrollo del embrión, éste puede tomar una coloración blanquecina, amarilla clara o amarilla oscura cuando el insecto está próximo a emerger. En campo es usual encontrar grandes cantidades de huevos en las yemas terminales de las ramas, éstos pueden observarse en diferente tiempo de desarrollo indicado por las diferentes coloraciones.

Posturas de C. eucalypti en puntas de ramas y axilas de las hojas
Ciclo de vida de Ctenarytaina eucalypti, en condiciones de laboratorio
Todas las ninfas recién emergidas son de color claro y con el transcurso de algunas horas toman el color característico de cada estado. En las ninfas de primer ínstar, la longitud del cuerpo (sin incluir las antenas) es en promedio de 0.4 mm. Son de color amarillo, con prominentes ojos rojizos. Inmediatamente después de su nacimiento, el individuo inicia la alimentación en las partes más tiernas de las yemas axilares.
En las ninfas de segundo ínstar, la longitud del cuerpo alcanza en promedio 0.5 mm, son de color amarillento y ya se observa la aparición de rudimentos alares. En el tercer ínstar alcanzan un tamaño promedio de 0.69 mm, con primordios alares desarrollados los cuales no alcanzan el primer segmento abdominal. En algunos individuos la región dorsal toma una coloración no generalizada de tono marrón. A partir de este estado se alimentan en otras partes del ápice de la planta como las láminas foliares (Fig. 2).
En el cuarto ínstar de desarrollo ninfal los rudimentos alares están bien desarrollados y alcanzan el segundo segmento abdominal, son en la mayoría de los casos de tono marrón opaco. En este estado la longitud promedio del cuerpo es de 1.01 mm; la producción de cera se hace ya muy evidente siendo a manera de filamentos blancos que recubren el cuerpo y dan refugio a los miembros de la colonia. Durante el quinto ínstar los rudimentos alares recubren más de la mitad del dorso abdominal, son de color marrón oscuro y tienen muy poca movilidad. El volumen abdominal y la longitud del cuerpo en la hembra es un poco mayor que en el macho, siendo de 1,57 mm y 1,28 mm, respectivamente.

Hojas jóvenes infestadas
Los adultos son alados, poseen gran movilidad y al ser perturbados, se desplazan rápidamente; de allí su nombre común de piojos brincadores. Poseen ojos compuestos protuberantes de color rojo, ocelos presentes sobre la parte dorsal de la cabeza al lado de cada ojo. Aparato bucal picador-chupador con pico corto trisegmentado, de color amarillo los dos primeros segmentos y marrón el segmento apical. Antenas setáceas con ocho segmentos, las cuales poseen una degradación de color de marrón, en su parte apical, a amarillo en su parte basal. Se aprecia diferencia en el tamaño entre el macho y la hembra, alcanzando esta última una longitud promedio de 2.26 mm mientras que el promedio para machos es de 1.76 mm. Patas caminadoras con coloración amarilla, fórmula tarsal 2:2:2, pretarso constituido por dos uñas y cojinete. Dos pares de alas transparentes con venación escasa, siendo la anterior un poco más grande y apergaminada que la posterior. El abdomen está constituido en ambos sexos por seis segmentos, que para el caso de los machos es menos voluminoso que en las hembras. Presenta color amarillo con una coloración marrón irregular superficial. La genitalia externa permite diferenciar claramente el macho de la hembra (Fig. 2).
Los adultos requieren un periodo de precópula de tres días después de los cuales la hembra puede aparearse con varios machos y con varias hembras para el caso de estos últimos. Se observó un periodo de preoviposición de aproximadamente 9 días y periodo de oviposición de 16 días durante los cuales cada hembra puede depositar hasta 10 huevos por día. Los huevos son puestos en las axilas de las hojas primordiales de los rebrotes de la planta, en promedio cada hembra genera 160 huevos, con un porcentaje de eclosión de 93.5%.
En las condiciones estudiadas, el ciclo de vida tiene una duración promedio de 149 días; es decir, que el insecto alcanza a completar de dos a tres generaciones por año, la cual es inferior a la registrada por otros autores que mencionan la ocurrencia de cada generación en periodos de un mes o mes y medio. Llama la atención la longevidad de los adultos que alcanza cerca del 50% del total, la cual en combinación con la condición alada del insecto así como su reconocida habilidad de desplazamiento, explica en parte la gran capacidad colonizadora del insecto, observada en los lotes infestados.
Características del daño de C. eucalypti
En el follaje joven de árboles de vivero, en los rebrotes de plantaciones taladas y en árboles de regeneración natural en la sabana de Bogotá y sus alrededores, se observan grandes poblaciones de C. eucalypti, los cuales excretan una mielecilla transparente y secretan filamentos algodonosos que pueden llegar a recubrir toda la colonia y en conjunto con las exuvias afectar la apariencia de los árboles de vivero y rebrotes jóvenes generando preocupación sobre todo en los viveros forestales que conlleva a la utilización de productos insecticidas.

Estados de desarrollo ninfales y adulto
Aun cuando el registro de hospederos está referido a varias especies de eucaliptos, en Colombia hasta ahora sólo se ha observado sobre E. globulus. Aunque en campo se pueden observar secamientos o retorcimientos de rebrotes sin que este daño sea generalizado, en los árboles evaluados en invernadero (Fig. 2) no se presentaron cambios estructurales en las ramas infestadas (retorcimientos, desecamientos y bifurcaciones) tales como los señalados para España y Portugal en donde este insecto es catalogado como plaga forestal de importancia (Cadahia 1980). Al realizar una comparación mediante análisis de variación de los promedios de peso seco/cmβ de las puntas de ramas infestadas contra las no infestadas obtenidos en cada tratamiento, no se detectaron diferencias estadísticamente significativas. Esto último no necesariamente evidencia que no haya efecto de la alimentación del insecto sobre la producción de biomasa, sino que más bien sugiere la necesidad de revisar una metodología más sensible para determinar el efecto micro y microscópico del ataque. Así mismo, al parecer las condiciones de crecimiento en invernadero favorecen un rápido desarrollo de tejido suculento que puede en un momento dado disimular por compensación el efecto nocivo que se esperaría observar ante una alta infestación con psílidos.
Son pocos los registros referentes al daño causado y las consecuencias por efecto de la alimentación de los psyllidae que, para el caso de los eucaliptos, ocurre solamente en el follaje joven y puede ser imperceptible si el hospedero es vigoroso y no está sometido a condiciones de estrés (Cadahia y Ruperez 1979). Otro factor a considerar en el desarrollo e impacto de las poblaciones en el follaje del eucalipto, es la ocurrencia de esclerofilia que determina la cantidad de nutrientes y contenido de agua. Las hojas en desarrollo son más suaves y contienen más nitrógeno y agua que las hojas maduras, siendo por lo tanto superiores desde el punto de vista nutricional y mecánicamente más fáciles de consumir para muchos herbívoros (Larson y Ohmart 1988, citados por Steinbauer et al. 1998). Dreisdat et al. (1999) observaron cómo las ninfas y adultos del psylido Glycaspis brimblecombei en varias especies de eucaliptos prefieren los brotes suculentos nuevos, estimulados por el exceso de nutrientes, especialmente de nitrógeno que ocurre luego de la fertilización con formulaciones de nutrientes de rápida absorción. Igualmente, condiciones de estrés favorecen la infestación ya que los niveles de nitrógeno se incrementan en el follaje cuando los eucaliptos están estresados favoreciendo la reproducción y sobrevivencia de sus poblaciones. El endurecimiento del follaje determina la abundancia de varias especies de psyllidae en E. blakely (Clark y Dallwitz 1974).
Aun cuando se ha profundizado en el sitio en que los psílidos toman el alimento del tejido foliar de eucaliptos, se tienen pocas evidencias sobre la ocurrencia de daños externos y las consecuencias sobre la productividad de la planta. En un estudio realizado con cuatro especies de psyllidae en follaje de eucalipto, Cardiaspina albitextura Taylor, Creiis costatus (Frogg) y Lasiopsylla rotundipennis Frogg, obtienen su alimento a partir del floema y parénquima de pequeños haces vasculares mientras que Glycaspis sp. se alimenta de floema mayores. Los daños visibles en las hojas sólo se observan con las especies Glycaspis sp. y Cardiaspina albitextura que ocasionan un marchitamiento similar a la senescencia natural, causando rompimiento del tejido de empalizada en el mesófilo de la hoja (Woodburn y Lewis 1973). Tal como lo indicaron Dalshten et al. (1996), Azevedo y Figo (1979), la infestación con C. eucalypti es más espectacular que dañina y por lo tanto el daño observado a consecuencia del ataque de los psyllidae en E. globulus es principalmente estético y la tolerancia varía entre las personas, las plantas afectadas y la localización de los cultivos. Así mismo, en forma general, la infestación en esta especie forestal cesa cuando el tejido de la hoja se endurece.
Enemigos naturales y pruebas preliminares de efectividad
El complejo de enemigos naturales encontrado en la zona de estudio estuvo representado únicamente por insectos depredadores. Se encontraron tres especies de la familia Syrphidae: Allograpta neotropica Curran (N Wyatt (NHM) det.), Ocyptamus sp. nr caldus (Walker) Syrphinae (N. Wyatt (NHM) det.) y Syrphus shorae Fluke (N Wyatt (NHM) det.). Este último sírfido se observó de forma esporádica. Se encontró también depredando sobre C. eucalypti, a una especie de crisopa parda: Hemerobius sp. (Neuroptera: Hemerobiidae), (P. Barnard (NHM) det.).
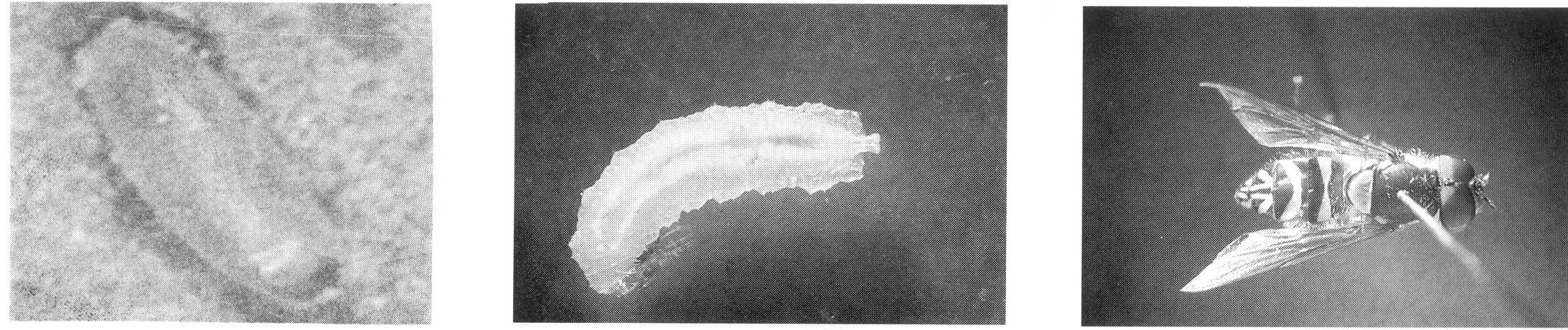
Huevo, larva y adulto de A. neotropica
A continuación se describen características morfológicas y biológicas útiles para el reconocimiento de cada uno de los enemigos naturales que se observaron para la especie en campo.
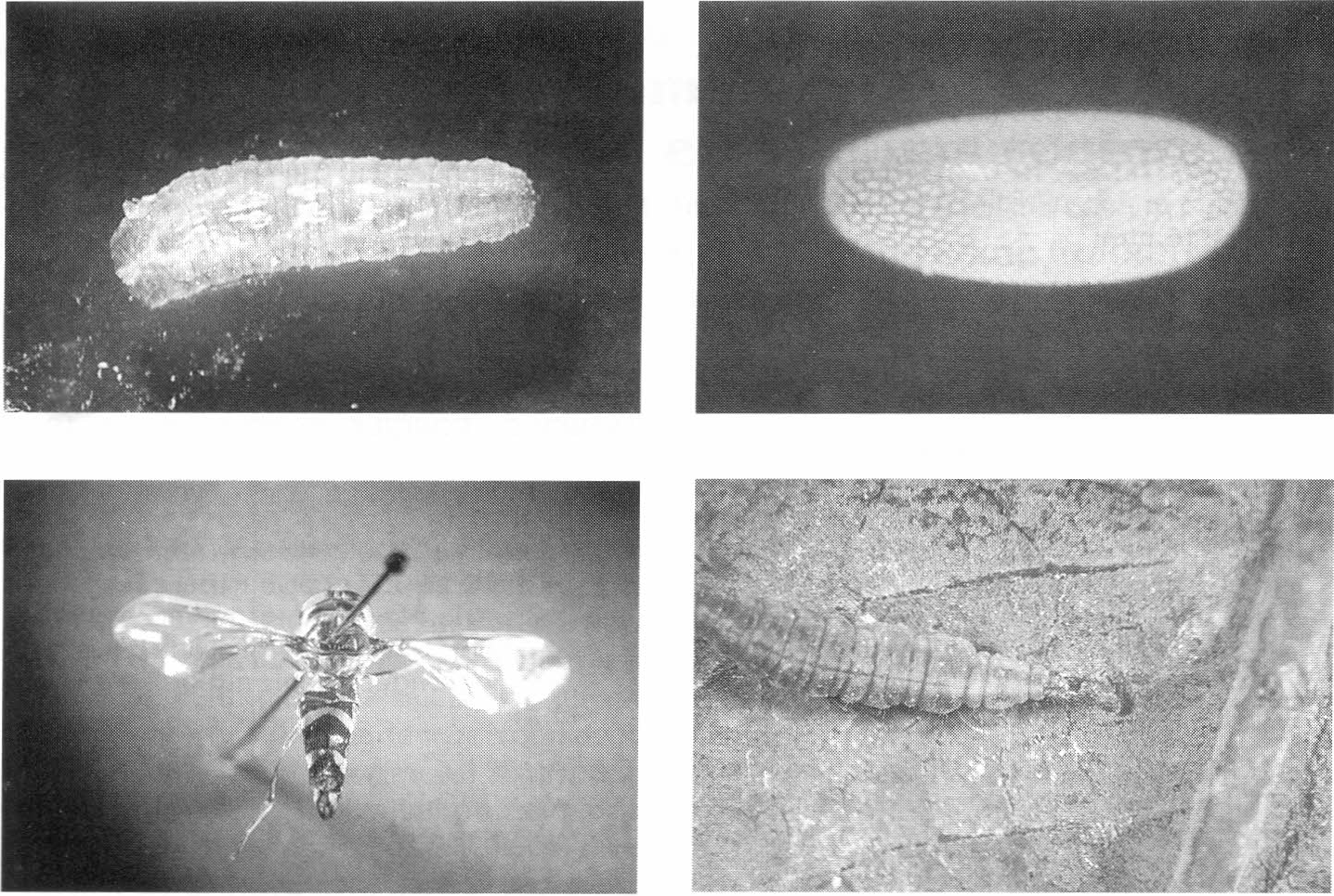
Larva y adulto de Ocyptamus sp.
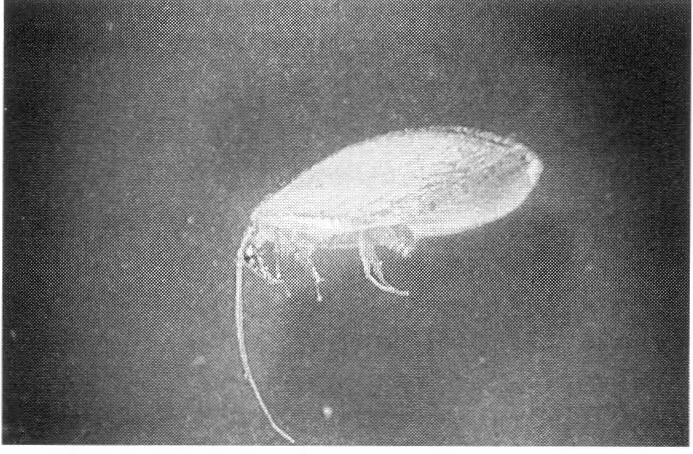
Huevo, larva y adulto de Hemerobius sp.
Durante los seguimientos efectuados únicamente se encontró control natural por parte de insectos depredadores, no se vieron parasitoides ni evidencias de ataque por microorganismos entomopatógenos.
En la figura 7 se compara el consumo promedio de presas en periodos de 24 horas por cada uno de los ínstares de desarrollo larval de A. neotropica, Ocyptamus sp. y Hemerobius sp. Al comparar, mediante análisis de variación y test de rangos múltiples (LSD), la efectividad de depredación en periodos de 24 horas, se encontró que A. neotropica y Ocyptamus sp. consumen igual número de presas de primer, segundo y tercer ínstar siendo en todo caso mayor que el consumo por parte de Hemerobius sp.
De los tres enemigos naturales evaluados en forma preliminar, se observó mejor capacidad depredadora con las especies Ocyptamus sp. y A. neotropica, presentando una buena adaptabilidad a los factores abióticos, buen potencial reproductivo y facilidad para la cría masiva. Siendo menos efectivo Hemerobius sp., no sólo por su bajo consumo sino también por su poca representación en la entomofauna asociada a E. globulus y por su baja capacidad para soportar condiciones ambientales poco favorables (lluvias fuertes).
Las tres especies poseen un ciclo de vida corto comparativamente con la especie plaga, lo que las hace depredadoras eficientes de C. eucalypti con las restricciones anteriormente expuestas para Hemerobius sp. La sincronización con la oferta alimenticia es buena para el caso de A. neotropica y Ocyptamus sp. ya que aproximadamente por una generación de C. eucalypti, se dan tres de los dípteros y aunque para Hemerobius sp. ocurre lo mismo estas ultimas son menos frecuentes en las ramas infestadas por C. eucalypti.
Por tratarse de una especie introducida es apenas lógico que el complejo de enemigos naturales observados corresponda a depredadores, cuya polifagia sobre chupadores de savia es ampliamente reconocida. La predominancia de la familia Syrphidae dentro del complejo de enemigos naturales de esta especie coincide con los registros de la literatura (Olivares 2000), aun cuando los géneros y especies registrados son propios de cada región. Considerando que los parasitoides son específicos, la posibilidad de obtener control por parte de éstos dependerá de su introducción a nuestro medio, tal como ha sido realizado en California, Francia e Irlanda con parasitoides introducidos desde Australia (Dahlsten 1996; Chauzat y Purvis 2000).
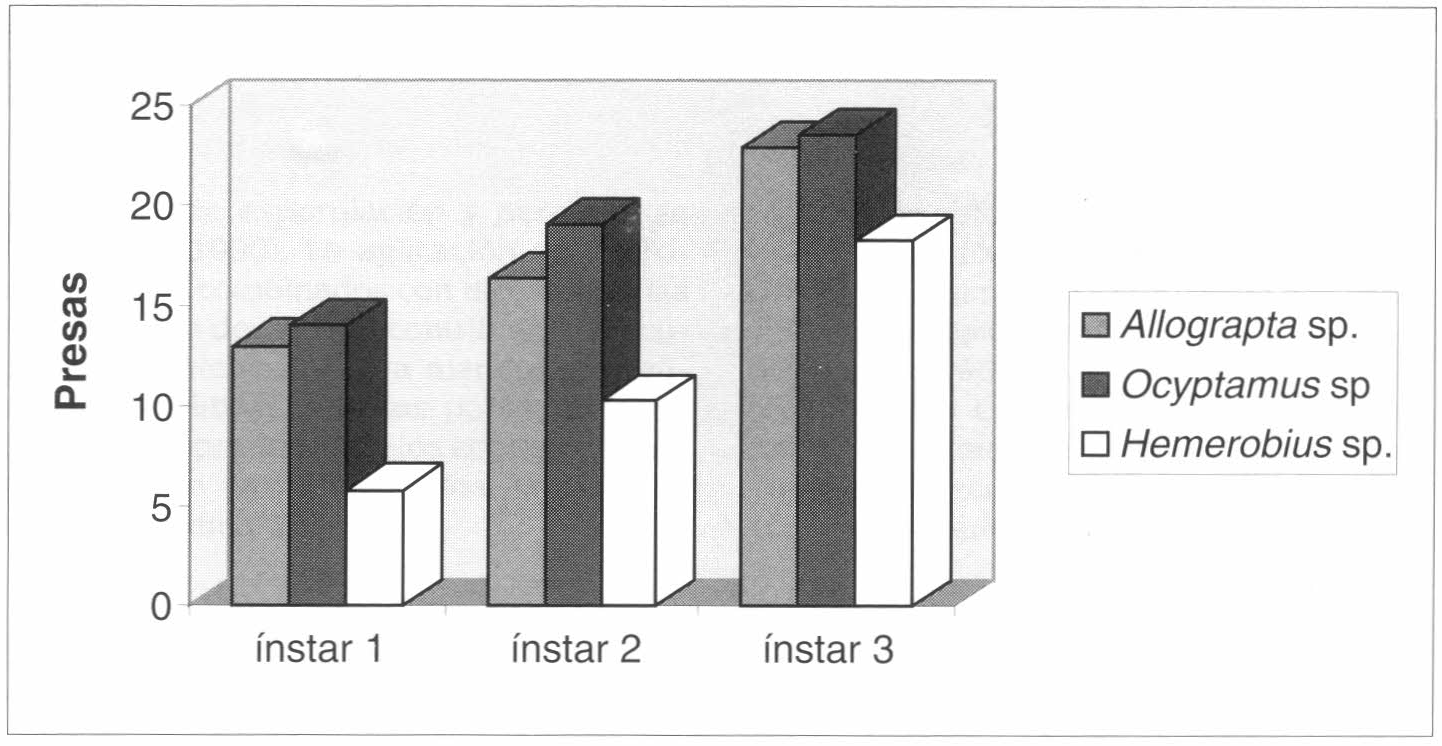
Consumo promedio en 24 horas, de presas de tres ínstares ninfales de C. eucalypti
Conclusiones y Recomendaciones
El pulgón del E. globulus fue identificado como Ctenarytaina eucalypti (Maskell) confirmando de esta forma la introducción al país de este insecto que durante algún tiempo se consideró plaga potencial para la reforestación en el país.
Bajo las condiciones climáticas evaluadas, el pulgón de E. globulus, Ctenarytaina eucalypti alcanza a completar durante el año dos y media generaciones durante las cuales presenta un alto potencial reproductivo, características morfológicas y hábitos que permiten catalogarlo como un insecto con gran capacidad de colonización y dispersión.
Ctenarytaina eucalypti se alimenta solamente de primordios foliares y hojas tiernas de E. globulus, por lo tanto la presencia e incidencia de las poblaciones está regulada en alto grado por el estado fisiológico del follaje, ya que una vez éste se endurece cesa la infestación del tejido.
Las poblaciones de C. eucalypti son reguladas en forma natural, principalmente por depredadores de las especies: Allograpta neotropica, Ocyptamus sp. nr. caldus y ocasionalmente por las especies Syrphus shorae y Hemerobius sp.
Allograpta neotropica y Ocyptamus sp. presentaron una capacidad de depredación interesante en condiciones de laboratorio y mejor comparativamente con Hemerobius sp., por lo que se recomienda profundizar en el estudio de las interrelaciones depredador - presa y su potencial como una posible forma de regulación biológica de C. eucalypti en el caso en que las infestaciones y las condiciones del ataque así lo ameriten.
