Abstract
The distribution of the most important whitefly species affecting annual crops was established in Ecuador and Colombia. The greenhouse whitefly Trialeudores vaporariorum (Westwood) and the biotypes A and B of Bemisia tabaci (Gennadius) were identified through RAPD with the primer OPA-04. T. vaporariorum was found in all tropical highlands and interandean valleys of Colombia and Ecuador attacking dry beans, snap beans, tomato and potato. The B biotype of B. tabaci was found throughout the Atlantic Coast of Colombia affecting cotton, tomato, melon, Brassica sp. and eggplant. Furthermore, it was the only species found along the coast of Ecuador. The distribution of the A biotype of B. tabaci was restricted to Córdoba, Sucre, Valle del Cauca, and Huila. This biotype seems to have been displaced by the B biotype, which is more aggressive. B. tabaci and T. vaporariorum seem to have well defined ecological niches but they can also coexist in certain areas like Valle del Cauca, Tolima and Huila. The distribution, according to the elevation, was as follows: the B biotype of B. tabaci was found between 0 and 890 masl, the A biotype between 50 and 1350 masl and T. vaporariorum between 600 and 2830 masl.
Keywords
Introducción
De las aproximadamente 1200 especies de moscas blancas descritas hasta ahora en América Central y el Caribe existen al me-nos 30 agrupadas en 15 géneros (Caballero 1992). No obstante, con base en criterios tales como su persistencia, densidad poblacional, ámbito de hospederos y distribución geográfica, se han distinguido Bemisia tabaci (Gennadius) y Trialeurodes vaporariorum (Westwood) como las más importantes económicamente en los trópicos (De Ponti et al. 1990). Ambas especies son cosmopolitas y polífagas de manera que B. tabaci se ha encontrado habitando 506 especies de plantas agrupadas en 74 familias (Greathead 1986) y T. vaporariorum en 249 especies de plantas (Vet et al. 1980). T. vaporariorum afecta los cultivos debido al daño mecánico que causa y a la excreción de melazas (Byrne et al. 1990) mientras que la importancia de B. tabaci radica principalmente en su capacidad para transmitir virus y por la ocurrencia de biotipos dentro de la especie. El biotipo B de B. tabaci, conocido por su agresividad (Perring et al. 1993), se registró por primera vez en Colombia en 1997 gracias a polimorfismos encontrados en patrones de bandas de esterasas y de RAPDs, inducción de plateado de hojas en Cucurbita spp. y por diferencias en su capacidad reproductiva en algunos hospedantes (Quintero et al. 1998).
Los problemas con moscas blancas han alcanzado magnitud mundial en los últimos años lo cual ha hecho que se dediquen esfuerzos a investigación básica y métodos de control. El control químico ha sido la herramienta principal de combate y su uso inadecuado ha conducido al desarrollo de resistencia de las moscas blancas a insecticidas (Buitrago et al. 1994; Dittrich et al. 1990; Anderson 1993) y a la resurgencia de plagas, entre otros (Cardona 1995). El marco conceptual que guía la investigación en insectos plaga es el manejo integrado de plagas (MIP) en el cual el primer paso es la identificación de dichos insectos (Maezler (1986) citado por Anderson (1992)). De esta forma, el trabajo de identificación de especies ofrece un mejor entendimiento del grupo de insectos pues la similitud de muchas especies de mosca blanca ha conducido a confusiones cuya consecuencia más negativa ha sido la aplicación indiscriminada de insecticidas sobre una multitud de especies así éstas no causen problemas serios en los cultivos (Hilje 1995).
En este trabajo se realizó la identificación de especies de moscas blancas en cultivos hortícolas de algunas regiones de Colombia y Ecuador, como parte de un plan de investigación encaminado a desarrollar programas de manejo integrado de estos insectos.
Materiales y Métodos
El área de muestreo comprendió lugares de Colombia y Ecuador identificados de la siguiente manera: trópico bajo (principalmente costas y regiones con altitudes menores de 400 msnm), valles interandinos localizados a altitudes entre 400 y 1000 msnm y trópico alto (zona Andina a alturas superiores a los 1000 msmn). En los sitios visitados se colectaron muestras de pupas y adultos para realizar la identificación morfológica y molecular de las moscas blancas así: las hojas infestadas con pupas se colocaron directamente en frascos plásticos en etanol al 70% y los adultos se tomaron con un aspirador bucal y se pusieron en tubos para microcentrífuga que contenían etanol al 70%. Se analizaron 214 muestras para las cuales se registraron datos de altura sobre el nivel del mar así como los nombres de los hospedantes afectados.
La caracterización morfológica de pupas se hizo de la siguiente manera: se revisó el material vegetal bajo microscopio estereoscopio y se colectaron 10 pupas las cuales luego de ser aclaradas se montaron permanentemente en bálsamo de Canadá. La identificación se hizo al microscopio de acuerdo con las claves morfológicas de Martin (1987) y Caballero (1992). Para la identificación molecular, los adultos se filtraron y se dejaron secar por 30 minutos hasta la evaporación del alcohol. Posteriormente se guardaron a -20°C por periodos cortos de tiempo (1 a 2 meses) y a -80°C por periodos largos (más de 2 meses). La extracción de ADN se hizo de hembras individuales según el método descrito por Quintero et al. (1998). El ADN de todas las muestras se amplificó mediante RAPD con el cebador OPA-04. La comparación con los testigos de las colonias de cría permitió la identificación de las bandas polimórficas y en consecuencia de las especies de moscas blancas. Para ello se utilizaron como testigos los biotipos A y B de B. tabaci criados sobre Phaseolus vulgaris L. (var. ICA Pijao) a 20-22°C y 40-50% HR, y T. vaporariorum criado también sobre P. vulgaris a 18°C y 70% HR (Quintero et al. 1998).
Resultados y Discusión
Existen hasta el momento dos técnicas de laboratorio que permiten identificar moscas blancas: la electroforesis de esterasas y la amplificación de ADN al azar (RAPD) (Quintero et al. 1998). Para este trabajo se escogió la técnica de RAPD que permite un manejo fácil de las muestras en el campo pues se pueden conservar directamente en alcohol sin necesidad de refrigerar.
Se procesaron en el laboratorio 214 muestras distribuidas de la siguiente forma: 47 colectadas en el trópico bajo, 51 en los valles interandinos y 116 en el trópico alto. Se realizó la amplificación del ADN de las muestras colectadas mediante RAPD utilizando el cebador OPA-04, el cual había mostrado mayor utilidad para la identificación de moscas blancas debido al alto grado de polimorfismo (Quintero et al. 1998). De esta forma se lograron distinguir los patrones de bandas característicos de B. tabaci biotipos A y B, y de T. vaporariorum, en comparación con los testigos (Fig. 1). Cuando se compararon las identificaciones morfológicas con las moleculares se encontró un 100% de coincidencia en los resultados. Además, los métodos resultaron ser complementarios pues, mientras la caracterización morfológica no permitió identificar biotipos de B. tabaci, esto se logró mediante RAPD.
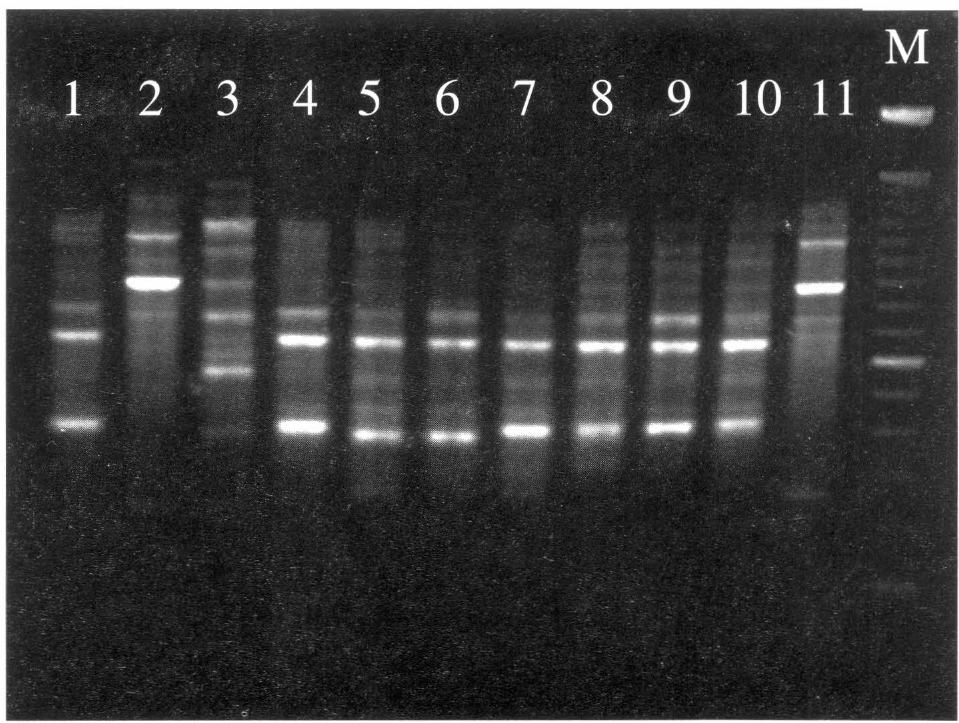
Identificación de moscas blancas mediante RAPD. Amplificación del cebador OPA-04. 1, T. vaporariorum; 2, B. tabaci biotipo A; 3, B. tabaci biotipo B; 4-10, T. vaporariorum (Valle del Cauca); 11, B. tabaci biotipo A (Valle del Cauca); M, marcador 100 pb
Luego de la identificación de todas las muestras, se pudo establecer la distribución geográfica de las especies de moscas blancas en las zonas visitadas. Así, los resultados mostraron la prevalencia de T. vaporariorum desde el norte de Ecuador continuando por la Zona Andina colombiana hasta los departamentos de Antioquia, Norte de Santander y el sur de Bolívar (Fig. 2). En cuanto a B. tabaci, la distribución de cada biotipo fue la siguiente: el biotipo B predominó al norte en la costa colombiana y en la costa ecuatoriana. También se encontró hacia el interior de Colombia en el Valle del Cauca, Tolima y Huila. En general el biotipo B ha ampliado su distribución en gran medida, lo cual ha conducido al desplazamiento y limitación del biotipo A a unas cuantas zonas aisladas de los departamentos de Córdoba, Sucre, Valle del Cauca y Huila (Fig. 2). En Córdoba se registraron ambos biotipos sobre tomate y berenjena: el biotipo A se encontró aislado hacia el centro del departamento (Tierra Alta). En Sucre en la localidad de Sampués se encontraron ambos habitando cultivos aledaños: el biotipo A en berenjena y el B en col.
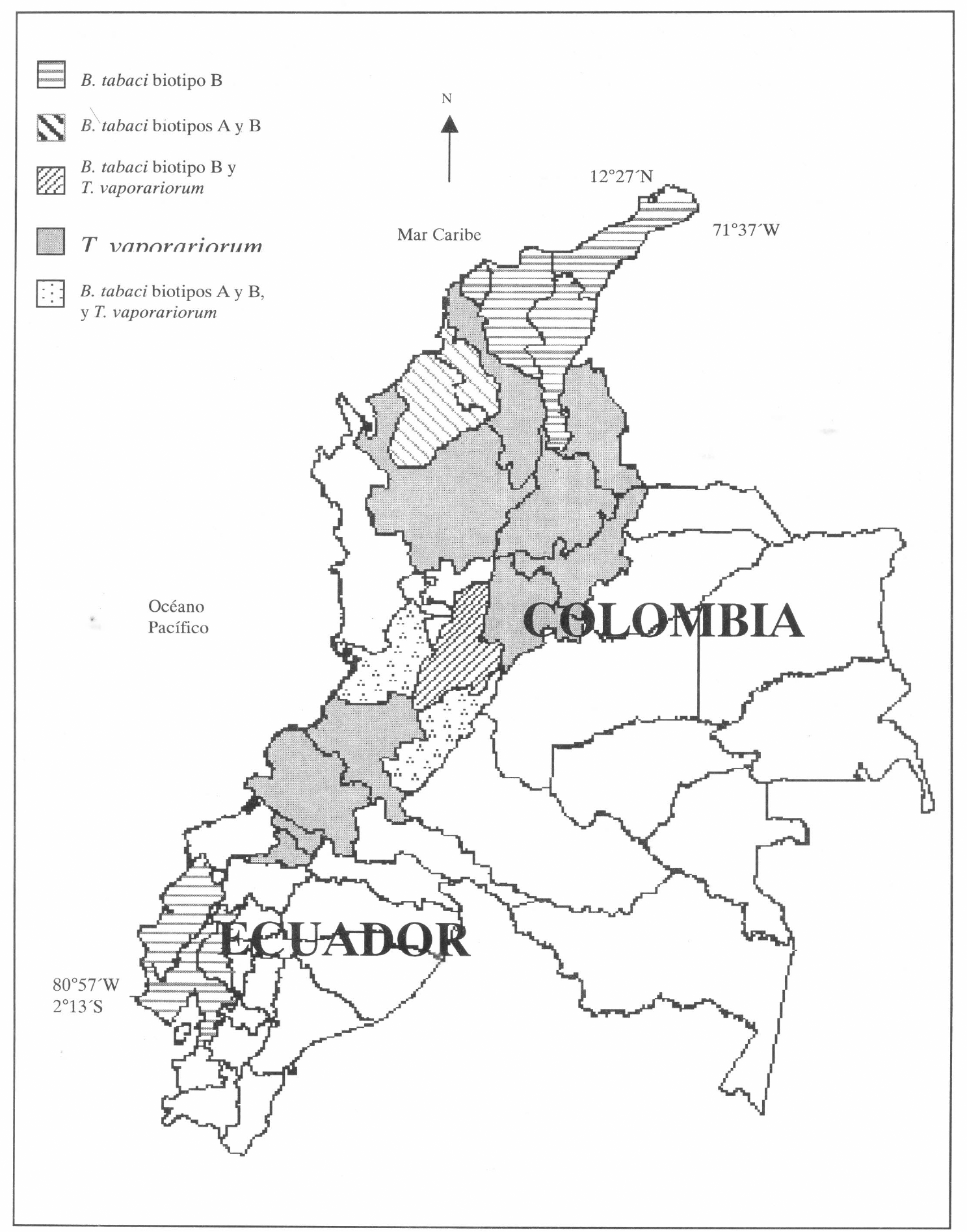
Distribución geográfica de especies y biotipos de mosca blanca en Colombia y Ecuador.
Al analizar la composición de especies de moscas blancas de acuerdo con las diferentes zonas ecológicas definidas para el estudio, se halló que la especie predominante en el trópico bajo fue el biotipo B de B. tabaci identificada en un 91.5% de las muestras colectadas principalmente en las costas de Ecuador y Colombia. El biotipo A ha sido casi completamente desplazado pues sólo se encontró en un 8.5% (Fig. 3). En los valles interandinos los biotipos A y B de B. tabaci así como T. vaporariorum se encontraron representados por 13.7%, 25.5% y 60.8%, respectivamente (Fig. 3). En cuanto al trópico alto (alturas mayores de 1000 metros) la única especie encontrada fue T. vaporariorum. En consecuencia, aunque B. tabaci y T. vaporariorum dominan áreas ecológicas muy distintas también se hallaron compartiendo nicho ecológico (Valle del Cauca, Tolima y Huila) (Fig. 2).
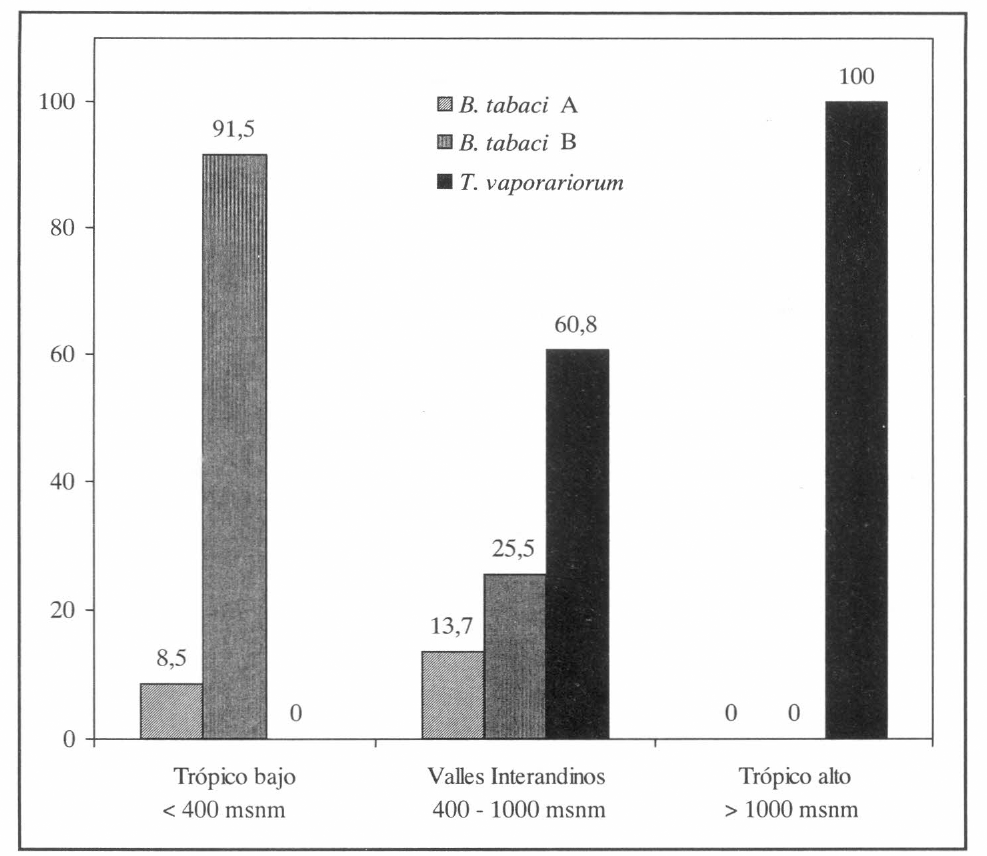
Composición de especies de moscas blancas en tres zonas ecológicas de Colombia y Ecuador.
De acuerdo con Byrne et al. (1990), el hombre ha transportado las moscas blancas a nuevos hábitats y también ha alterado los ambientes favoreciendo la supervivencia de especies de moscas blancas en áreas donde usualmente no podrían desarrollarse. Esto podría explicar el hecho de que T. vaporariorum, que tradicionalmente se había encontrado por encima de los 800 msnm (Caballero 1992) esté ahora a partir de 600 msnm (Huila, tomate y tabaco). La altura máxima a la cual se registró esta especie fue 2830 msnm (Cundinamarca, papa). El biotipo A de B. tabaci estuvo desde 50 msnm (Córdoba, berenjena) hasta 1350 msnm (Poinsettia, Valle del Cauca). El rango de alturas a las que se halló el biotipo B fue de 0 hasta 890msnm (Fig. 4).
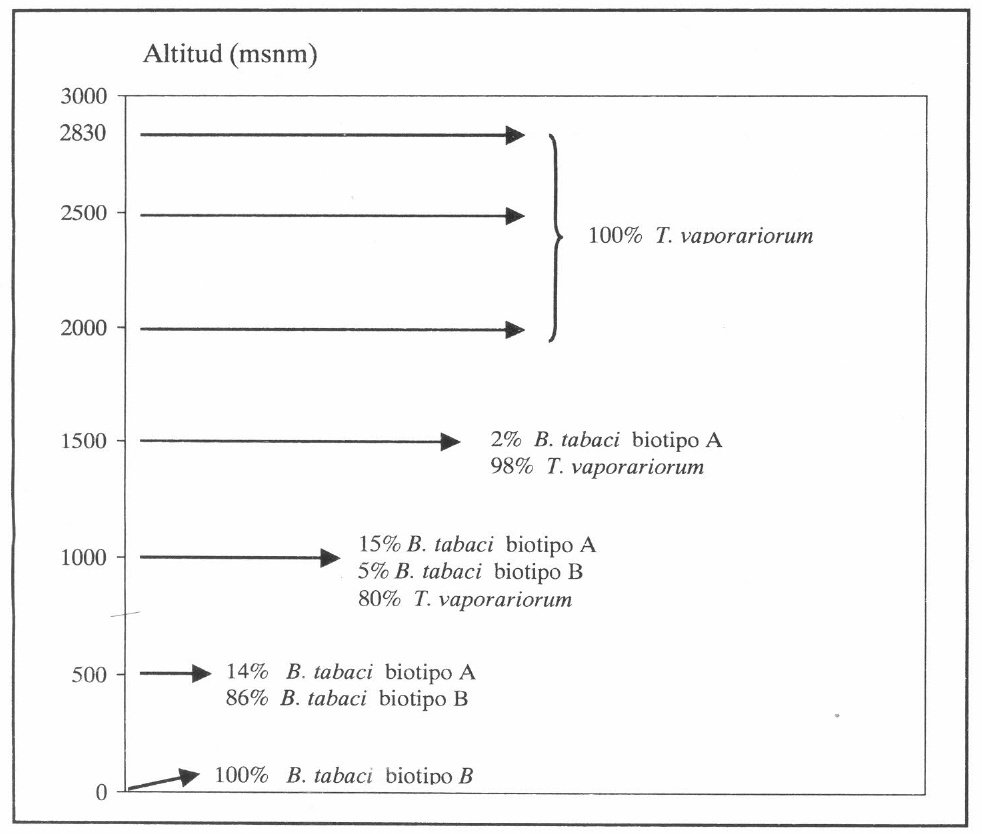
Distribución altitudinal de especies y biotipos de mosca blanca en Colombia y Ecuador.
Los cultivos más importantes afectados por moscas blancas se destacan en la Tabla 1. El biotipo A se encontró en seis: berenjena, tomate, tabaco, soya, brócoli y poinsettia. Los hospedantes del biotipo B incluyeron nueve especies de plantas: algodón, berenjena, Cucurbita spp., col, melón, fríjol lima, pepino, sandía, tomate, y tabaco. Este último se registró por primera vez como hospedante reproductivo del biotipo mencionado. T. vaporariorum se encontró atacando ocho cultivos en los valles interandinos y regiones del trópico alto así: fríjol, habichuela, pepino, tabaco, tomate, Cucurbita spp. y papa.
Principales cultivos afectados por moscas blancas en la zona Andina de Colombia y Ecuador
Se ha insinuado en la literatura la posible existencia de biotipos dentro de T. vaporariorum (Bink-Moenen y Mound 1990). Por ello se hizo un análisis más riguroso de las muestras colectadas con el fin de buscar biotipos de esta especie. Inicialmente se comparó el patrón de esterasas de insectos procedentes en su mayoría del Valle del Cauca. Se encontró una muestra polimórfica para estas isoenzimas, originaria de Carmen de Viboral (Antioquia). Sin embargo, luego de evaluar mediante RAPD algunos cebadores que han sido útiles en la identificación de biotipos de B. tabaci (OPA-04, OPA-07, OPA-11 y OPA-17 (Gawel y Bartlett 1993), no se hallaron polimorfismos en el ADN de los individuos evaluados. En un estudio posterior, se escogieron muestras de fríjol representativas de las diferentes regiones donde se encontró T. vapo-rariorum. Luego de la extracción, el ADN se amplificó utilizando la metodología descrita para RAPD utilizando los cebadores ya citados. Nuevamente, no se encontraron diferencias entre los patrones de bandas amplificados por lo cual se concluyó que hasta el momento no se han encontrado biotipos de T. vaporariorum (Fig. 5).
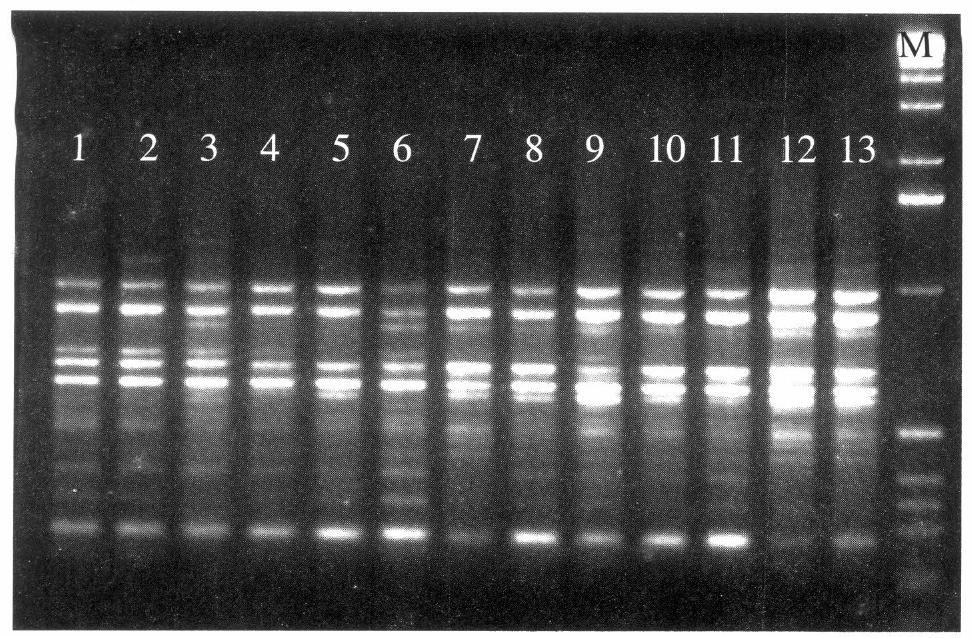
Amplificación del cebador OPA-07 en individuos de T. vaporariorum colectados sobre fríjol en varias localidades de Ecuador (1 y 2) y Colombia (3-11); 12, testigo de T. vaporariorum (Fusa); 13, testigo de T. vaporariorum (Tenerife).
La identificación de moscas blancas mediante RAPD permitió establecer la distribución de las especies más importantes a lo largo de la zona Andina Colombiana y Ecuatoriana, y los principales cultivos semestrales que afectan. La información generada es parte fundamental de un plan de investigación encaminado a desarrollar programas de manejo integrado de estos insectos.
