Abstract
Objective:
The present review aims to assess the clinical efficacy and safety of the α-1-adrenergic antagonist prazosin as primary pharmacologic treatment for post-traumatic stress disorder (PTSD).
Method:
A systematic review was performed using keywords (i.e., prazosin, α-1-adrenergic antagonist, α-1-blocker, post-traumatic stress disorder) in the databases PubMed/Medline (1966–May 2016), Embase (1966–May 2016), ScienceDirect (1823–May 2016), OvidSP (1946–May 2016) and Nature (1845–May 2016). To be considered for inclusion, studies had to test the efficacy of prazosin either alone or added to ongoing treatment in adults with PTSD, use validated tools to assess and monitor the disorders, allow comparisons on the basis of univariate analyses (i.e., p-values of t-tests and effect sizes) and list the identified adverse reactions.
Results:
12 studies were included: 5 randomized controlled trials, 4 open-label prospective trials and 3 retrospective file reviews. The evaluation concerned 276 patients exposed to civilian trauma (19%) or war trauma (81%). Prazosin significantly decreases trauma nightmares, avoidance, hypervigilance and improves patient status in all studies. No significant difference of blood pressure was observed at the end of trials.
Conclusions:
Beyond the methodological and clinical biases of these studies, the present review not only confirms the effectiveness and good tolerability of prazosin, but also suggests its possible use as primary pharmacologic treatment for PTSD. Uncertainties remain, however, regarding the prescription modalities and dosages.
Introduction
L’état de stress post-traumatique (ESPT) représente une modalité évolutive fréquente, fortement comorbide et potentiellement chronique en l’absence de traitement, et constitue un enjeu de santé publique majeur. 1,2 En population générale, la prévalence vie entière de l’ESPT en Amérique du Nord (Etats-Unis & Canada) varie selon les études de 6,4 à 9,2%, 1,3 –9 contre 1,9% en Europe, 10 les femmes présentant des prévalences 2 à 3 fois supérieures à celles des hommes. En populations à risque, les prévalences les plus élevées (de 30 à plus de 50%) concernent des survivants de combats, de génocides ou d’internements arbitraires. 1 La prévalence vie entière de l’ESPT chez les vétérans nord-américains varie, selon les études, de 6 à 31%. 11 –13
Classé dans le DSM-5 parmi les troubles liés à des traumatismes ou à des stress, l’ESPT est un état morbide sévère lié à une exposition à des évènements traumatogènes (i.e., mort violente ou accidentelle, blessure grave, violence sexuelle ou menace pour l’intégrité physique, etc.) en tant que victime, mais aussi en tant que témoin, parent, personne proche ou dans un cadre professionnel (cluster A). 1,9
Selon les critères du DSM-5,
1
l’ESPT se caractérise par quatre syndromes spécifiques (clusters B-E) similaires à ceux du DSM-IV:
9
le syndrome de répétition ou de reviviscence caractérisé par des intrusions conscientes (i.e., reviviscences diurnes, souvenirs répétitifs et envahissants, cauchemars traumatiques ou épisodes dissociatifs). Ce syndrome est associé à une forte réactivité physiologique. le syndrome d’évitement pouvant se manifester sur les plans affectifs, cognitifs, comportementaux et physiologiques. le syndrome d’émoussement, associé à des cognitions négatives persistantes, une modification de l’humeur, une auto-dévalorisation, un état émotionnel négatif (i.e., peur, horreur, colère, culpabilité, honte), un désintérêt pour les activités habituelles, et un repli sur soi. Un autre aspect de ce syndrome, partie intégrante du cluster C (syndrome d’évitement/émoussement) dans le DSM-IV,
9
est l’émoussement des émotions qui peut aller jusqu’à une insensibilité émotive (détachement des affects). le syndrome d’hypervigilance (i.e., hyperstimulation, état d’alerte permanent, réactions de sursaut exagérées) souvent associé à des troubles du comportement (i.e., irritabilité, conduite auto- et/ou hétéro-agressive, violence), de la concentration et du sommeil.
Les symptômes (critères B-E) doivent, comme dans le DSM-IV, durer plus d’un mois (critère F), induire une détresse ou une altération significative, entre autre, du fonctionnement socioprofessionnel (critère G) et ne pas être dus à une substance ou un autre état pathologique (critère H). 1,9
Les troubles peuvent s’accompagner de symptômes non spécifiques (e.g., crises d’angoisse aiguës et récurrentes, épisodes dépressifs, phobiques, obsessionnels ou hystériques, troubles psychosomatiques, conduites à risque, abus impulsifs et compulsifs, troubles alimentaires et addictions). 1,9,14
L’ESPT représente une modalité évolutive fréquente, invalidante, fortement comorbide et potentiellement chronique en l’absence de traitement. 2
Le diagnostic repose sur une anamnèse spécifique et des symptômes bien répertoriés. L’utilisation d’outils d’aide au diagnostic permet une évaluation rapide des patients. Ces outils, de même que d’autres plus spécialisés, permettent d’explorer différents aspects de la pathologie. Seuls seront mentionnés, ici, les outils cités dans la présente étude. Couramment utilisé, le questionnaire Clinician Administered PTSD Scale (CAPS) 15 permet de dépister un ESPT selon les critères du DSM-IV. D’usage tout aussi courant, les échelles PTSD Checklist-Civilian version (PCL-C) 16 et Clinical Global Impression scale (CGI) 17 évaluent respectivement la sévérité des symptômes et l’amélioration ressentie par le patient. Dans la présente étude, les niveaux de détresse psychologique et de dépression sont caractérisés respectivement par le test Profile Of Mood States (POMS) 18 et l’échelle Hamilton Depression Rating Scale (HDRS) 19 . L’hyperéveil émotionnel est évalué grâce à l’échelle Non-Nightmare Distressed Awakenings scale (NNDA). 20 Le test Emotional Stroop Word test (ESW) 21,22 évalue quant à lui les effets cognitifs de l’hypervigilance. Enfin, les échelles Pittsburgh Sleep Quality Index (PSQI) 23 et PTSD Dream Rating Scale (PDRS) 24 évaluent respectivement la qualité du sommeil et les rêves, cette dernière distinguant les contenus pathologiques évocateurs d’ESPT des contenus normaux. Des explorations du sommeil et de la vigilance complètent généralement ces évaluations. 25
Les troubles psychologiques identifiés sont sous-tendus par des mécanismes neurobiologiques complexes impliquant de nombreuses voies. 2,14 Bien que n’étant qu’un élément d’un système complexe, le système noradrénergique est largement impliqué dans la symptomatologie de l’ESPT. 2 La noradrénaline joue non seulement un rôle central dans les niveaux d’alerte, la vigilance, l’attention, la réponse cardiovasculaire, mais également dans l’encodage émotionnel et la consolidation mnésique de l’évènement traumatique. 2,26,27 La plupart des symptômes seraient liés à une hyperactivité noradrénergique (hyperadrénergie). 2,14,26 –31 Des liens ont pu être établis, notamment, entre la dissociation péritraumatique (facteur de risque témoignant d’une dérégulation des mécanismes neurobiologiques de réponse au stress) et l’encodage mnésique au niveau du système limbique et du cortex préfrontal, mais également entre l’hyperéveil émotionnel et psychophysiologique et l’activation de l’axe hypothalamo-hypophyso-surrénalien. 2,32 –35 L’imagerie fonctionnelle montre des altérations du réseau des émotions (i.e., activation de l’amygdale, dysfonction de l’hippocampe et du cortex frontal). 26,36,37
De par ses projections avec l’amygdale, l’hippocampe, le cortex préfrontal et la formation réticulée, le locus coeruleus (LC), une des principales structures noradrénergiques cérébrales, active la vigilance et l’attention dans les situations d’alerte et régule la peur et l’anxiété (figure 1). 2,30,38,39 D’autres connexions avec les noyaux du raphé et les noyaux paraventriculaires (NPV) de l’hypothalamus font du LC un acteur majeur de la régulation du cycle veille-sommeil. 40,41 Des dysfonctionnements à ce niveau expliqueraient les reviviscences nocturnes sous forme de cauchemars traumatiques. 38 Lors d’un stress, l’activation du LC entraîne une libération de catécholamines. 26,42 Un excès d’activation catécholaminergique induit l’émergence de symptômes centraux (hyperéveil, flashbacks, mémorisation émotionnelle, etc.) et périphériques (tachycardie, hypertension, etc.). 26 L’activation des NPV active l’axe corticotrope et induit la production de corticotropin-releasing factor (CRF). 26 Il en résulte une importante libération de noradrénaline et de cortisol, le CRF activant la libération de noradrénaline lors d’un stress. 26,27,42 Un excès de noradrénaline dans le liquide céphalo-rachidien et des taux de cortisol bas sont observés chez les patients souffrant d’ESPT. 2,14,43 –45 Un défaut d’activation corticotrope constituerait un facteur de risque. 26,46,47 Des déficits d’inhibition cérébrale peuvent également expliquer les dysfonctionnements observés. C’est particulièrement le cas pour les dysfonctions de la neurotransmission GABAergique, l’acide gamma-aminobutyrique (GABA), un neurotransmetteur, inhibant les transmissions adrénergiques et assurant l’essentiel de l’inhibition cérébrale. 26 Des taux bas en GABA après un évènement traumatique détermineraient le développement de syndromes psycho-traumatiques. 26,27 Le tonus opiacé endogène ainsi que la production du neuropeptide Y (NPY) protégeraient du stress. 2,26,27,30,48
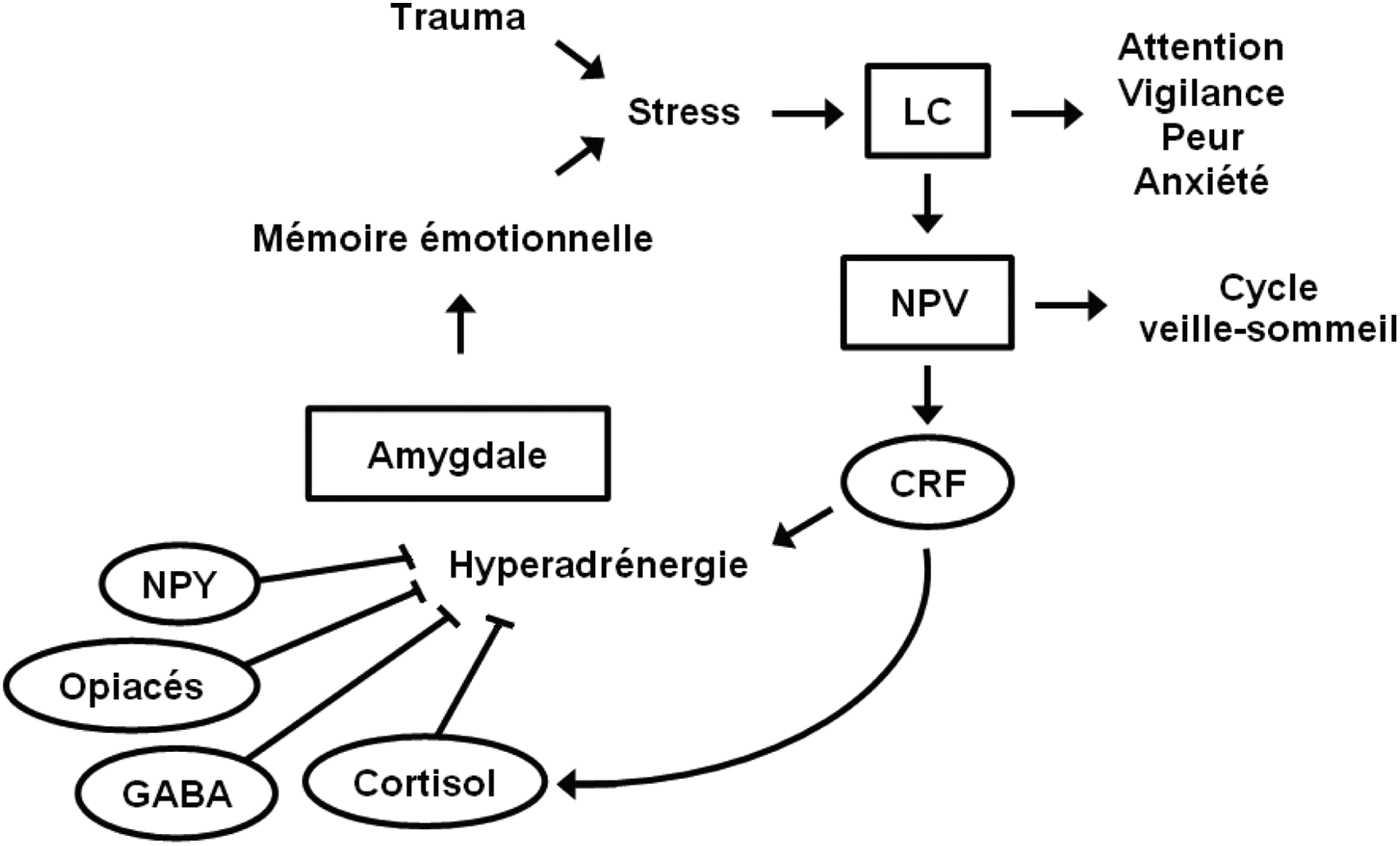
Neurobiologie du trauma dans un modèle de stress
Une augmentation du métabolisme de la dopamine est aussi observée. 14 Son élévation plasmatique et l’augmentation de son excrétion urinaire seraient corrélées avec la sévérité de l’ESPT, notamment l’intensité des reviviscences. 14,49
Une altération de la modulation sérotoninergique expliquerait les conduites d’évitement et la dimension dépressive. 50,51 L’apparition d’une dépression dans les mois suivant un traumatisme sous-tendrait un état chronique. 52
Il n’existe pas de traitement pharmacologique standard de l’ESPT. Les traitements médicamenteux ciblent généralement les troubles anxieux et dépressifs. Les anxiolytiques sont rapidement efficaces, mais présentent, entre autres, un risque de pharmacodépendance à long terme. 53 –55
Le système sérotoninergique cérébral étant impliqué dans la régulation du stress et de l’anxiété, des inhibiteurs sélectifs de la recapture de la sérotonine (ISRS), tels que la paroxétine et la sertraline, de même que des inhibiteurs de la recapture de la sérotonine et de la noradrénaline (IRSN), tels que la venlafaxine, sont généralement prescrits en première intention. 14,56 –60 Toutefois, seuls 20-50% des patients présentent une rémission. 58,60 –69 Ces inhibiteurs sont, d’autre part, inadaptés au traitement des intrusions. 68,70
Des antagonistes β-adrénergiques (β-bloquants) ont été testés. 71 –74 Un β-bloquant non sélectif, le propranolol, réduit l’encodage émotionnel et le renforcement mnésique de l’évènement traumatique, et présente de fait une certaine efficacité préventive. 2,68,71,72,75 –79 Le propranolol s’avère toutefois d’usage limité pour le traitement des syndromes d’évitement et d’hypervigilance en cas de troubles constitués. 73,78,80 Des β-1-bloquants sélectifs, tels que le betaxolol, seraient plus indiqués. 73,80 Les β-bloquants sont cependant fréquemment associés à des troubles du sommeil. 70,81,82
Des agonistes α-2-adrénergiques, tels que la clonidine et la guanfacine (antihypertenseurs sédatifs), permettraient de réduire l’hyperactivité noradrénergique. 2,60,70,83 –85 Ces substances pourraient toutefois potentialiser ou majorer un état dépressif latent. 82
Un antagoniste α-1-adrenergique (α-1-bloquant) utilisé depuis de nombreuses années dans le traitement de l’hypertrophie bénigne de la prostate 86 et de l’hypertension 87 , la prazosine, présente un intérêt majeur. Cette molécule induit une diminution des réponses noradrénergiques cérébrales lors de stress et améliore significativement la qualité du sommeil. 25,45,88 –91 La prazosine est notamment recommandée par le Département des Anciens Combattants des Etats-Unis et par certains auteurs pour le traitement de troubles sévères du sommeil ou de cauchemars traumatiques résistants à des traitements psychothérapeutiques et/ou médicamenteux conventionnels. 45,70,77,92 –94 Les taux de prescription progressent aux Etats-Unis (>30% dans certains centres). 95,96
L’intérêt de la prazosine ne se limite cependant pas à ces seules indications. 97 Selon les formes galéniques et/ou les régimes posologiques adoptés, d’autres symptômes, notamment diurnes, peuvent être atténués.
La prazosine est généralement commercialisée sous deux formes galéniques distinctes: Absorbée par voie orale sous sa présentation classique à libération immédiate (type Minipress®, Pfizer Inc., New York), la prazosine présente un pic plasmatique à 30 minutes et une demi-vie plasmatique de 2 à 4 heures.
45,82,98,99
En début de traitement, le pic plasmatique peut induire des hypotensions orthostatiques du fait d’un effet vasodilatateur lié au blocage des récepteurs α-1-post-synaptiques (effet de première dose).
82,99
Institué à faible dose, le traitement doit être progressivement augmenté par paliers, sous surveillance médicale (posologies de 0,5 à 20 mg/jour).
82,99
Après absorption orale d’une dose thérapeutique de prazosine à libération prolongée (type Alpress® LP, Pfizer Inc., New York), au contraire, les concentrations plasmatiques de prazosine s’élèvent progressivement, sans pics plasmatiques, après un temps de latence de 4 heures.
82,99
Elles se maintiennent en plateau de la 6e à la 24e heure, puis décroissent lentement.
82,99
Les taux plasmatiques sont proportionnels aux doses absorbées (2,5 à 20 mg/jour).
82,99
Les contraintes de suivi n’en sont que plus réduites.
Le traitement peut faire l’objet d’une utilisation prolongée. 31,91
La présente revue vise à évaluer l’efficacité clinique et la sécurité d’emploi de la prazosine, comme traitement pharmacologique principal de l’ESPT.
Méthode
Recherche documentaire
Une recherche a été effectuée au moyen d’une combinaison de mots clés et d’opérateurs booléens [(“prazosin” OR “alpha-1-adrenergic antagonist” OR “alpha-1-blocker”) AND (“post-traumatic stress disorder” OR “PTSD”)] sur tous les champs interrogeables dans les bases de données PubMed/Medline (1966–mai 2016), Embase (1966–mai 2016), ScienceDirect (1823–mai 2016), OvidSP Journals@Ovid Full Text (1946–mai 2016) et Nature (1845–mai 2016).
Critères d’inclusion et d’exclusion
Pour être retenues, les études devaient: (i) tester l’efficacité de la prazosine seule ou associée à un traitement antérieur maintenu inchangé; (ii) concerner des adultes présentant un ESPT récent ou constitué, diagnostiqué selon des critères DSM; (iii) évaluer objectivement les troubles avant et après traitement à l’aide d’outils diagnostiques reconnus; (iv) permettre d’établir des comparaisons valides sur la base d’analyses univariées (i.e., moyennes, écarts-types, valeur p du test t et taille d’effet); et (v) lister les effets indésirables recensés.
Classement méthodologique
Les études retenues ont été classées en trois catégories de qualité décroissante (I-III): (I) essais cliniques contrôlés et randomisés portant sur des échantillons représentatifs, (II) études de cohorte et cas-témoins, (III) séries cliniques et études de cas, les études pouvant changer de classe selon leur qualité méthodologique. 100 –102
Analyse statistique
Une analyse différentielle des données entre le début et la fin des essais a été effectuée au moyen du test t de Student. Les différences sont jugées statistiquement significatives, si p < 0,05. Les tailles d’effet correspondent au d de Cohen, 103 rapport entre la différence des moyennes et l’écart-type commun. Une valeur d de 0,2 correspond à un effet faible, 0,5 à un effet moyen et 0,8 à un effet fort. La taille d’effet souligne l’importance clinique d’un effet, par-delà sa significativité statistique.
Résultats
Au total, 1094 références ont été recensées dans les bases de données (PubMed/Medline: 125; Embase: 378; ScienceDirect: 238; OvidSP Journals@Ovid Full Text: 336; Nature: 17). Après élimination de doublons, 796 références ont été répertoriées. Au vu des titres et résumés des publications, 784 références ne répondant pas aux critères requis (e.g., éditoriaux, lettres, commentaires, actes de congrès, revues, articles hors thématique, etc.) ont été successivement exclues. Une revue des 12 références restantes a permis de recenser une référence supplémentaire. Parmi les 13 références présélectionnées, 12 études ont été retenues: 5 essais randomisés, contrôlés par placebo et réalisés à l’aveugle; 25,31,89,90,104 (ii) 4 essais prospectifs ouverts; 105 –108 et (iii) 3 analyses rétrospectives de dossiers médicaux. 28,109,110 On dénombre 2 études de classe I, 31,90 7 études de classe II, 25,89,104 –107,109 et 3 études de classe III. 28,108,110 Une étude de 2012, 111 présentant un biais de sélection (critères diagnostiques non satisfaits dans 42% des cas), 102 a été exclue.
Les évaluations ont concerné 276 patients répondant aux critères du DSM-IV. Ces patients ont été confrontés à des évènements traumatiques de la vie civile (19%) ou de guerre (81%). Les caractéristiques sociodémographiques des populations incluses dans les études considérées sont synthétisées dans le tableau 1. 52% des patients sont des vétérans (n = 144), 29% des militaires en activité (n = 80), 11% des civils (n = 29) et 8% des réfugiés (n = 23). Les femmes représentent 19% de l’effectif total (n = 52). Sauf à une exception, 31 le statut professionnel et le niveau d’éducation des patients ne sont pas précisés dans les études.
Caractéristiques sociodémographiques des patients inclus dans les études cliniques.
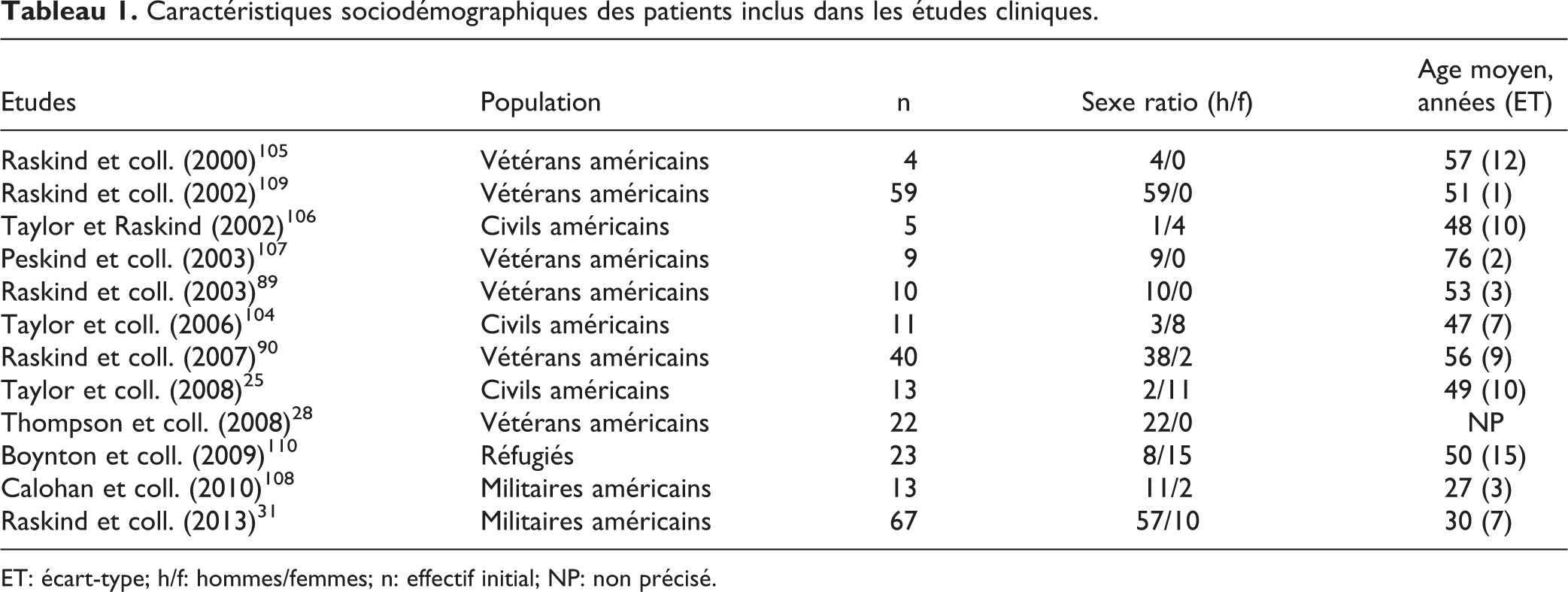
ET: écart-type; h/f: hommes/femmes; n: effectif initial; NP: non précisé.
Les principaux résultats sont rassemblés dans le tableau 2. La prazosine dite classique (à libération immédiate) a été utilisée dans toutes les études. Dans la majorité des cas, l’administration d’une seule dose de prazosine au coucher, suffit à réduire significativement les symptômes nocturnes (i.e., cauchemars traumatiques, troubles du sommeil). La prise d’une seconde dose, le matin, permet toutefois de majorer les effets et de cibler d’autres symptômes, notamment diurnes. 31
Analyse comparée des effets de la prazosine sur la symptomatologie de l’état de stress post-traumatique.
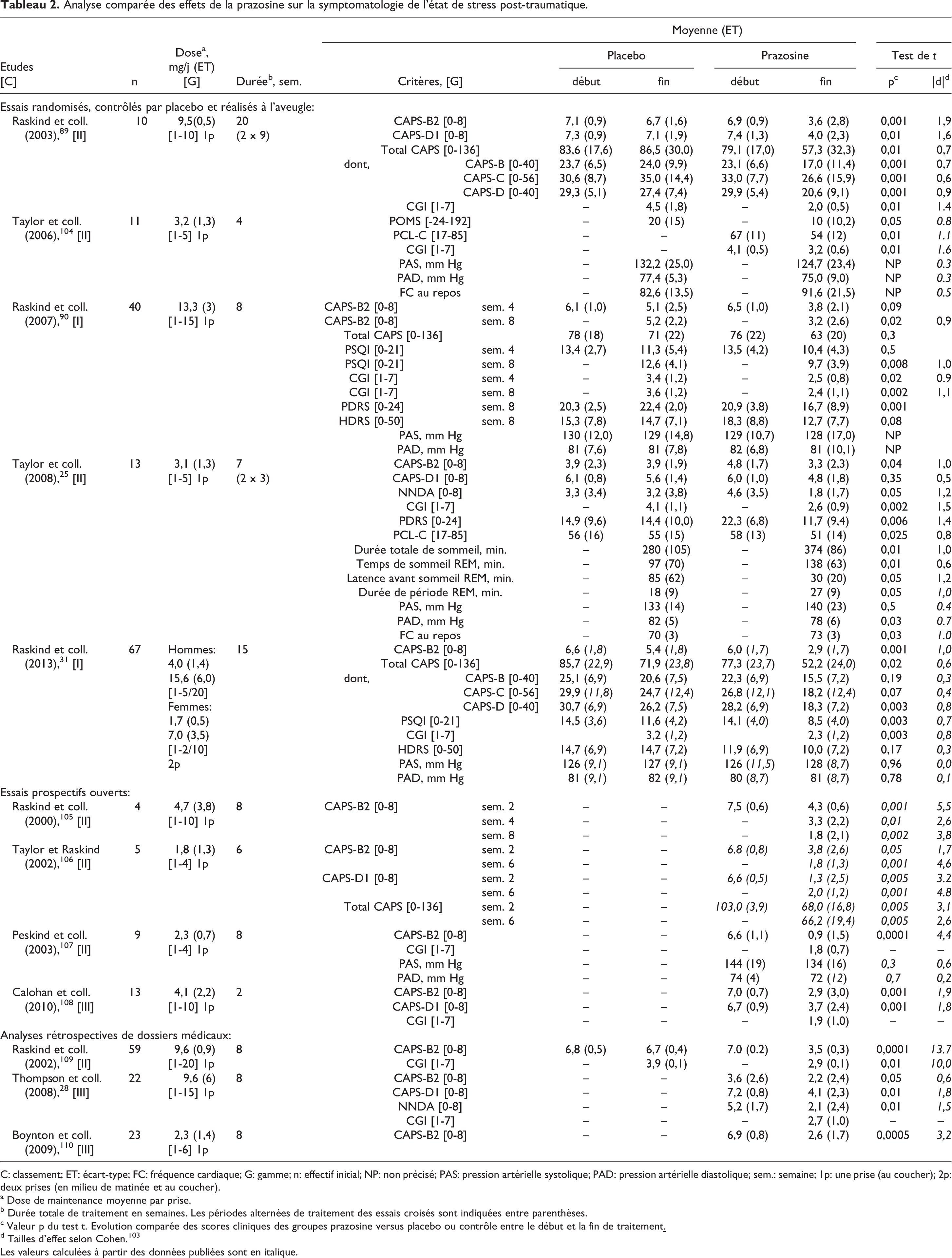
C: classement; ET: écart-type; FC: fréquence cardiaque; G: gamme; n: effectif initial; NP: non précisé; PAS: pression artérielle systolique; PAD: pression artérielle diastolique; sem.: semaine; 1p: une prise (au coucher); 2p: deux prises (en milieu de matinée et au coucher).
a Dose de maintenance moyenne par prise.
b Durée totale de traitement en semaines. Les périodes alternées de traitement des essais croisés sont indiquées entre parenthèses.
c Valeur p du test t. Evolution comparée des scores cliniques des groupes prazosine versus placebo ou contrôle entre le début et la fin de traitement
d Tailles d’effet selon Cohen. 103
Les valeurs calculées à partir des données publiées sont en italique.
Aucune variation significative de la tension artérielle systolique n’est constatée à l’issue des essais.
Les effets indésirables et les traitements psychopharmacologiques concomitants sont respectivement recensés dans les tableaux 3 et 4. Le traitement est bien toléré et présente un ratio efficacité/effets indésirables et une sûreté d’emploi à long terme satisfaisants. 45,92,112,113 Les principaux effets secondaires recensés sont des vertiges (en début de traitement), des nausées et des céphalées. 45,82,99,102,112,113 Un avis cardiologique préalable est recommandé pour les patients présentant des antécédents cardiovasculaires. 45
Effets indésirables recensés en cours de traitement.

n: effectif initial; NP: non précisé; pl/pr: placebo/prazosine.
a en début de traitement.
b patients sous placebo ayant souhaité être placés sous prazosine.
c dont 4 (3/1) sous antihypertenseur.
d dont 2(2/0) pour effet indésirable et 2(1/1) ayant souhaité être placés sous prazosine.
Traitements psychopharmacologiques concomitants.
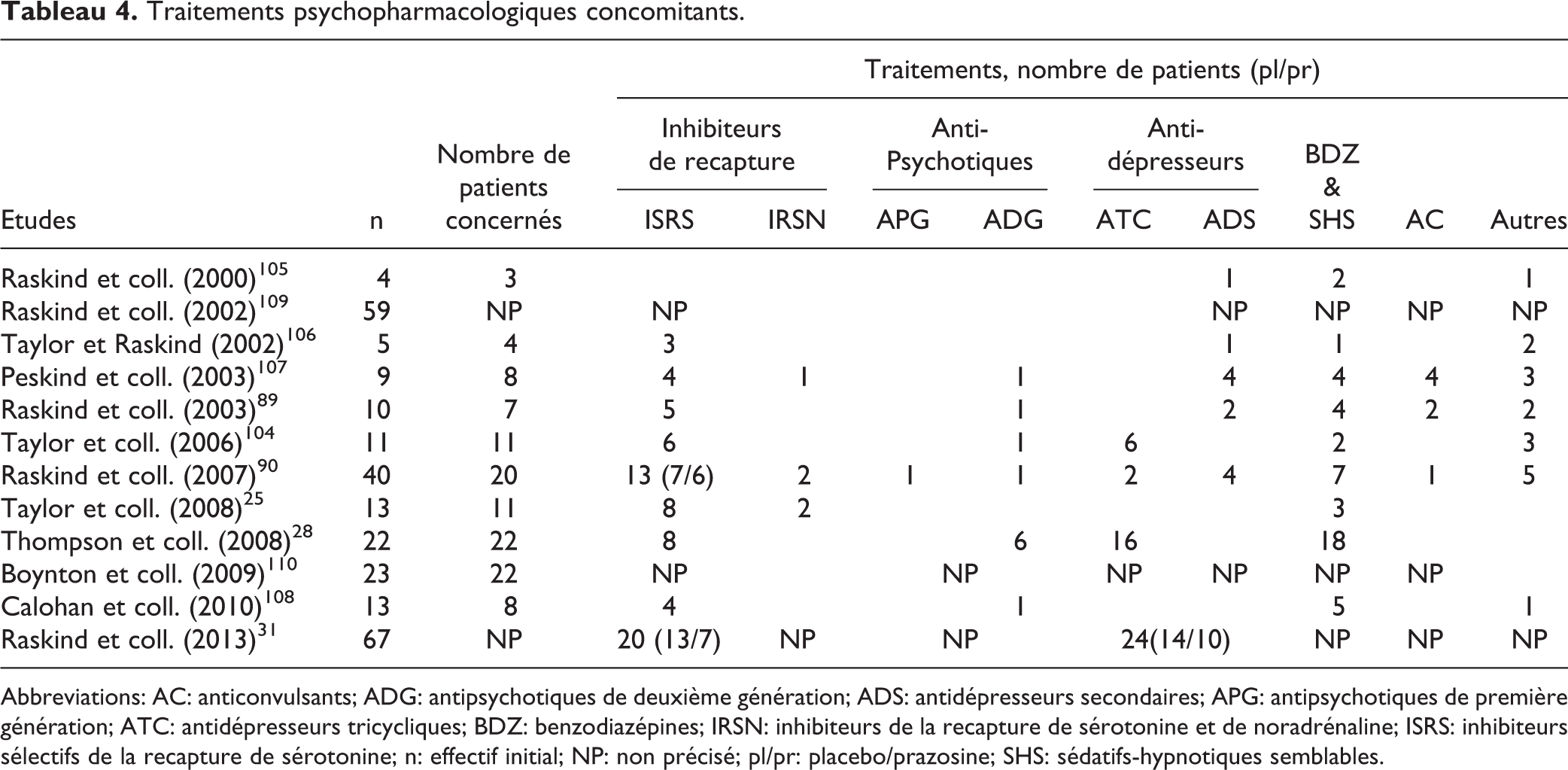
Abbreviations: AC: anticonvulsants; ADG: antipsychotiques de deuxième génération; ADS: antidépresseurs secondaires; APG: antipsychotiques de première génération; ATC: antidépresseurs tricycliques; BDZ: benzodiazépines; IRSN: inhibiteurs de la recapture de sérotonine et de noradrénaline; ISRS: inhibiteurs sélectifs de la recapture de sérotonine; n: effectif initial; NP: non précisé; pl/pr: placebo/prazosine; SHS: sédatifs-hypnotiques semblables.
Discussion
Les résultats obtenus sont prometteurs et suggèrent une utilisation possible de la prazosine comme traitement pharmacologique principal de l’ESPT, y compris dans un contexte opérationnel. Cependant, la validité et la portée des résultats sont limitées par l’hétérogénéité des critères d’inclusion et d’exclusion, la diversité des objectifs de recherche, l’adoption de régimes posologiques différents, la multiplicité des critères de jugement, la variabilité de l’échantillonnage, la faible diversité des investigateurs et des groupes étudiés, des variations liées à l’âge, au sexe, et à des interactions médicamenteuses,
Hétérogénéité des critères d’inclusion et d’exclusion
Les résultats des études retenues demeurent difficilement comparables entre eux du fait de critères d’inclusion et d’exclusion différents. Les populations étudiées ne s’avèrent donc pas homogènes. Sept études introduisent des critères de gravité comme critères d’inclusion: (i) PCL-C ≥ 40 et CAPS-B2 (“rêves répétitifs de l’évènement provoquant un sentiment de souffrance”) et -D1 (“difficulté à s’endormir ou à rester endormi”) ≥ 4 pour Taylor et coll. (2008); 25 (ii) CAPS ≥ 80 et CAPS-B2 ≥ 4 pour Taylor et Raskind; 106 (iii) CAPS ≥ 50 and CAPS-B2 ≥ 5 pour Raskind et coll. (2013); 31 (iv) CAPS-B2 et -D1 ≥ 5 pour Raskind et coll. (2007); 90 (v) CAPS-B2 ≥ 5 pour Raskind et coll. (2002) et Peskind et coll.; 107,109 et (vi) CAPS-B2 ≥ 6 pour Raskind et coll. (2000,2003). 89,105 Sept études, celles de Raskind et coll. (2000,2002,2007,2013), Taylor et coll. (2006,2008) et Taylor et Raskind, excluent les patients présentant une dépendance à une substance active. 25,31,90,104 –106,109 Les études de Raskind et coll. de 2007 et 2013 excluent de surcroît ceux présentant une comorbidité psychiatrique. 31,90 Toutes les études autorisent le maintien de traitements pharmacologiques et psychothérapeutiques concomitants, à l’exclusion des thérapies cognitivo-comportementales. Ces traitements sont demeurés inchangés durant les essais.
Pour la majorité des patients étudiés, la durée d’évolution de l’ESPT n’est pas connue. 102 On ignore, d’autre part, la symptomatologie initiale, de même que l’éventuelle existence de complications liées à l’ESPT. 102
Diversité des objectifs de recherche
Les études recensées évaluent essentiellement l’effet de la prazosine sur les cauchemars traumatiques (scores CAPS-B2), le sommeil (scores CAPS-D1 et PSQI) et les rêves (scores PDRS). Les études de Thompson et coll. et Taylor et coll. de 2008 s’intéressent de plus à l’hyperéveil émotionnel (scores NNDA), cette dernière évaluant de surcroît la qualité du sommeil. 25,28 La baisse des niveaux de sévérité (scores PCL-C et CAPS) et l’amélioration ressentie par les patients (scores CGI) n’étant pas l’objet premier de ces études, ces dernières n’ont dès lors pas pour objectif l’optimisation des résultats s’y rapportant.
Contrairement aux autres études, l’essai de Taylor et coll. de 2006 ne vise pas à caractériser l’effet de la prazosine sur les reviviscences et les troubles du sommeil associés, mais à évaluer les niveaux de détresse et la réactivité psychologique des patients (scores POMS et ESW). 104
Adoption de régimes posologiques différents
La prazosine est administrée dans tous les essais sous sa présentation classique. De manière à prévenir, chez certains patients, tout risque d’hypotension orthostatique en début de traitement, une faible dose initiale (1 mg) est prescrite dans toutes les études. L’étude de Taylor et coll. de 2008 exclut d’entrée les patients présentant des troubles orthostatiques (2/18; 11%). 25 La posologie (une dose au coucher) est ensuite progressivement augmentée suivant différents schémas d’administration jusqu’à obtention d’un effet thérapeutique (ou indésirable), puis maintenue constante en deçà d’un seuil prédéfini jusqu’au terme du traitement. Les doses requises, présentées dans le tableau 2, sont fonction des populations concernées et de l’effet escompté: (i) scores CGI ≤ 2 pour Taylor et Raskind; 106 (ii) réduction d’1 point (sur 5) de l’item PCL-C « rêves de l’évènement provoquant un sentiment de souffrance » pour Taylor et coll. (2006); 104 (iii) amélioration significative des scores NNDA pour Thompson et coll. (2008); 28 et (iv) absence de cauchemars traumatiques ou réduction substantielle des symptômes nocturnes pour les autres études. En l’absence de données physiques relatives aux patients, aucune dose moyenne rapportée au poids n’a pu être calculée.
Bien qu’efficace pour le traitement des cauchemars traumatiques, la prise d’une seule dose de prazosine dite classique au coucher ne suffit pas à soulager d’autres symptômes durant la journée. Les régimes posologiques adoptés sous-estiment de fait le potentiel thérapeutique réel de la prazosine. 31,114
Multiplicité des critères de jugement
Les multiples critères de jugement utilisés et l’absence de critère de jugement principal rendent les comparaisons difficiles entre essais.
Variabilité de l’échantillonnage
Le nombre de patients ayant participé à chacune des études retenues varie de 4 à 67. Les effectifs restreints (petits échantillons) limitent la puissance statistique des analyses. Les effectifs nécessaires n’ont pas au préalable été estimés.
Faible diversité des investigateurs et des groupes étudiés
Les études ont été menées pour la plupart par un même groupe de chercheurs. Des vétérans et des patients civils américains constituent l’essentiel des populations étudiées. Aucune étude multirégionale n’a été recensée. 95,96
Variations liées à l’âge, au sexe et à des interactions médicamenteuses
A tolérance équivalente, les posologies peuvent varier de 1 à 10, voire 15 mg et plus au coucher. 45 Les femmes s’avèrent particulièrement sensibles au traitement. 31,110 Des sujets jeunes présentant un ESPT récent requièrent généralement des doses moindres que des vétérans âgés présentant d’importantes comorbidités. 107,115 Des pharmacocinétiques différentes, des récepteurs α-1-adrénergiques de densité ou affinité variables, et des interactions médicamenteuses pourraient expliquer ces variations. 107 Difficile dès lors de définir une posologie optimale. 45
Une moindre efficacité apparente de la prazosine a pu être mise en évidence chez des patients sous ISRS. 31 Elle serait imputable aux effets des ISRS sur le sommeil (i.e., réduction du sommeil paradoxal, souvent associée à une augmentation de l’éveil, puis du sommeil lent). 31,116 –119
L’hétérogénéité méthodologique et clinique observée entre les études rend, de fait, toute méta-analyse inappropriée, car non fiable. 120
Conclusions
En dépit de ces limitations, les effets décrits de la prazosine confirment son efficacité et sa bonne tolérance. La possible utilisation de cet α-1-bloquant comme traitement pharmacologique principal de l’ESPT demeure envisageable. Toutefois, au vu des incertitudes qui demeurent quant aux modalités de prescription du traitement et aux posologies, de nouvelles études s’avèrent nécessaires.
Footnotes
Remerciements
Les auteurs tiennent particulièrement à remercier les réviseurs anonymes pour leurs remarques et suggestions constructives.
La présente revue a été rédigée dans le contexte de l’activité professionnelle de ses auteurs, sans aucun financement spécifique. Les auteurs déclarent ne pas avoir de conflits d’intérêts en relation avec cet article.
Les analyses et conclusions présentées sont celles des auteurs et ne reflètent pas nécessairement les avis de l’institution à laquelle ils appartiennent.
Declaration of Conflicting Interests
The author(s) declared no potential conflicts of interest with respect to the research, authorship, and/or publication of this article.
Funding
The author(s) received no financial support for the research, authorship, and/or publication of this article.
